
| 实验序号 | 滴定管液面起始读数 | 滴定管液面终点读数 |
| 1 | 1.32mL | 23.36mL |
| 2 | 2.26mL | 24.22mL |
分析 (1)依据C=$\frac{1000ρω}{M}$计算浓盐酸的物质的量浓度,然后依据稀释前后溶质的物质的量不变计算所需浓盐酸的体积,据此选择合适的量筒;
配制0.200mol•L-1的盐酸溶液500mL应选择500ml容量瓶;
依据配制一定物质的量浓度溶液的一般步骤排序;
(2)先判断数据的合理性,然后NaOH溶液的平均体积,然后根据HCl~NaOH求氢氧化钠的物质的量浓度;
(3)依据中和滴定正确操作解答;
(4)根据c(待测)=$\frac{C(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差.
解答 解:(1)浓盐酸的物质的量浓度=$\frac{1000×36.5%×1.20}{36.5}$=12.0mol/L,设需要浓盐酸的体积为:V,则0.200mol•L-1×500ml=12.0mol/L×V,解得V=
8.3ml,所以应选择10ml量筒;
配制0.200mol•L-1的盐酸溶液500mL应选择500ml容量瓶,将溶液转移到500ml容量瓶中配置;
配制一定物质的量浓度溶液的一般步骤为:计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶,所以正确的顺序为:A B D E C F;
故答案为:b; 8.3mL; 500mL容量瓶;A B D E C F;
(2)两次消耗的NaOH溶液的体积为22.04mL,21.96mL,均有效,盐酸溶液的平均体积为22.00mL,
HCl~NaOH
1 1
0.200mol•L-1×22.00mL c(NaOH)×20.00mL
解得:c(NaOH)=0.22mol/L;
故答案为:0.22 mol/L;
(3)A.滴定过程中,眼睛注视锥形瓶颜色变化,故错误;
B.滴定过程中由于摇动锥形瓶使少许溶液溅起沾在瓶内壁,为使测定结果正确,可用少许蒸馏水将其冲入锥形瓶内的溶液中,保证锥形瓶中所含溶质全部反应,故正确;
C.容量瓶和滴定管都带有塞子,为防止漏液,试用前需要检查是否漏水,故正确;
D.向锥形瓶中移取NaOH溶液前,用少许NaOH溶液润洗锥形瓶2~3次,导致待测液体积增大,则加入的标准液偏多,溶液浓度偏大,故错误;
故选:BC;
(4)A.滴定过程中不小心将一滴溶液滴在锥形瓶外,导致消耗的标准液偏多,结果偏大;
B.滴定结束时,发现在滴定管尖嘴处有小气泡,导致所加的标准液偏小,结果偏小;
C.滴定结束后仰视滴定管液面读数,导致消耗的标准液的体积偏大,结果偏大;
D.溶液褪色立即读数,摇动锥形瓶后看到溶液红色复出,过早判断滴定终点,导致所加标准液偏小,结果偏小;
E.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,直接加入标准液进行滴定,导致所加的标准液偏大,结果偏大;
故选:ACE.
点评 本题考查了一定物质的量浓度溶液的配置和酸碱的中和滴定,熟悉配制一定物质的量浓度溶液原理和步骤,熟悉中和滴定的原理是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铜片、铁片、FeCl3溶液组成的原电池 | |
| B. | 石墨、铁片、Fe(NO3)3溶液组成的原电池 | |
| C. | 银片、铁片、Fe(NO3)2溶液组成的原电池 | |
| D. | 铁片、铜片、Fe2(SO4)3溶液组成的原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
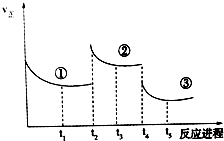 已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )
已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1,向密闭容器中加入2mol SO2和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是 ( )| A. | t2~t3时间段,平衡向逆反应方向移动 | |
| B. | t4时刻改变的条件是减小压强 | |
| C. | 平衡状态①和②,SO2转化率相同 | |
| D. | 平衡状态①和②,平衡常数K值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蓝矾 玻璃 无色的刚玉 | B. | 汽油 液氯 醋酸 | ||
| C. | 石蜡 纯盐酸 王水 | D. | 干冰 铝热剂 铁触媒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、CuSO4、HCl、KNO3 | B. | HCl、KOH、NaCl、Na2SO4 | ||
| C. | Ca(OH)2、Na2CO3、NaCl、HCl | D. | NaNO3、MgCl2、KCl、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、CH4都属于极性键的非极性分子 | |
| B. | C、N、O、F 电负性依次减小 | |
| C. | 基态铜(Cu)原子的电子排布式为[Ar]3d94s2 | |
| D. | 价电子构型为3s23p4的粒子其电子排布图为: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
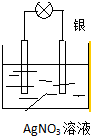 利用化学反应将存储在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量.
利用化学反应将存储在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1160 | B. | 2308 | C. | 1441 | D. | 2320 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com