
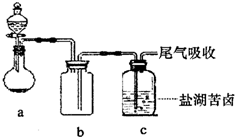
用如右图所示气体发生装置可以制取SO2(两种方法)和氯化氢(两种方法)气体,分别写出有关化学反应的化学方程式。
(1)制SO2(氧化还原反应) ;制SO2(复分解反应) 。
(2)制HCl的化学方法: ;制HCl的物理方法:烧瓶中盛 ,分液漏斗中盛 。
(3)如果撤去酒精灯,此装置可用于制H2、CO2、H2S及O2,如果用于制O2,烧瓶中盛 ,分液漏斗中盛 ,所发生反应的化学方程式为 。
(1)Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
Na2SO3+H2SO4 ![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
(2)NaCl+H2SO4(浓) ![]() NaHSO4+HCl↑
NaHSO4+HCl↑
浓盐酸 浓H2SO4
(3)MnO2 H2O2 2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(1)浓H2SO4具有强氧化性,与Cu或木炭粉在加热条件下反应被还原为SO2,因此可用浓H2SO4的氧化性来制取SO2。H2SO3不稳定,在加热条件下易分解,可通过强酸制弱酸得到H2SO3,再加热使其分解制SO2。
(2)实验室制取HCl是利用浓H2SO4的高沸点性,NaCl与浓H2SO4在加热条件下制得HCl气体。物理方法制HCl是利用了浓盐酸的挥发性,浓H2SO4吸水有利于HCl的溢出(注意浓H2SO4与其他液体混合时一般是向其他液体中慢慢滴加浓H2SO4)。
(3)实验室制O2是固体与固体在加热条件下的反应,而题目要求撤去酒精灯,因此不能用实验室方法来制取。本题可利用H2O2的不稳定性,易分解来制取O2。


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
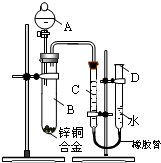 某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.查看答案和解析>>
科目:高中化学 来源: 题型:
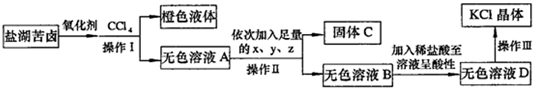
甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。甲+乙![]() 丙+丁
丙+丁
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水。
① 若甲为块状固体,丙为可燃性气体,其分子内既含有极性键又含有非极性键。则丙的电子式是 。
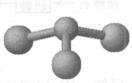
②若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示,丙具有漂白性。则甲中Cl元素的化合价是 。
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水。
① 若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
② 若丙和丁都可在一定条件下还原![]() ,此反应的化学方程式是 。
,此反应的化学方程式是 。
③ 若甲是由N和O元素组成的气态物质,呈红棕色。将3.36 g![]() 加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是 。
加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是 。
(3)Hofmann依据上述转化关系测定氨分子的组成。现用如右图所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至![]() 处。
处。
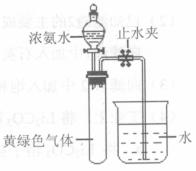
① 滴下浓氨水一段时间后,试管内发生反应的化学方程式是 。
② 证明试管内“不再反应”的实验操作和现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。甲+乙丙+丁
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水。
① 若甲为块状固体,丙为可燃性气体,其分子内既含有极性键又含有非极性键。则丙的电子式是 。
②若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示,丙具有漂白性。则甲中Cl元素的化合价是 。
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水。
① 若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
② 若丙和丁都可在一定条件下还原,此反应的化学方程式是 。
③ 若甲是由N和O元素组成的气态物质,呈红棕色。将3.36 g加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是 。
(3)Hofmann依据上述转化关系测定氨分子的组成。现用如右图所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至处。
① 滴下浓氨水一段时间后,试管内发生反应的化学方程式是 。
② 证明试管内“不再反应”的实验操作和现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com