
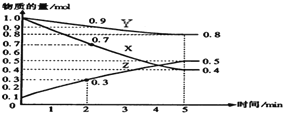
分析 (1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
(2)根据v=$\frac{\frac{△n}{V}}{△t}$计算;
(3)2min~5min之间X物质的量随时间发生变化未达到平衡状态;
解答 解:(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,
且△n(X):△n(Y):△n(Z)=0.6mol:0.2mol:0.4mol=3:1:2,则反应的化学方程式为:3X+Y?2Z,
故答案为:3X+Y?2Z;
(2)反应开始至2min时v(Z)=$\frac{\frac{0.3mol-0.1mol}{2L}}{2min}$=0.05mol•(L•min)-1,
故答案为:0.05mol•(L•min)-1;
(3)图象分析可知2min~5min之间X物质的量随时间发生变化未达到平衡状态,X的正反应速率比逆反应速率大,
故答案为:大.
点评 本题考查化学平衡图象分析题目、反应速率概念,题目难度不大,注意分析各物质的量的变化曲线,、化学方程式的判断方法.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:推断题
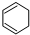 $\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$
$\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$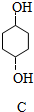 $\stackrel{O_{2}/Cu}{→}$
$\stackrel{O_{2}/Cu}{→}$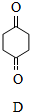
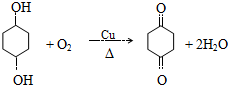 .
.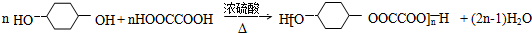 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaBr2 | B. | CaCl2 | C. | MgCl2 | D. | MgF2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蚕丝、羊毛、棉花的主要成分都是蛋白质 | |
| B. | 纤维素、油脂、蛋白质都能水解,但水解产物不同 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )
NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )| A. | NPG的分子式为C5H12O2 | B. | NPG沸点比乙二醇的高 | ||
| C. | NPG一定条件下能发生消去反应 | D. | NPG的氧化产物可发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
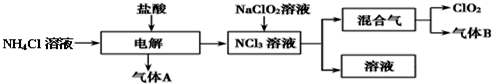
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种 | B. | 五种 | C. | 六种 | D. | 七种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com