
 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$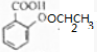 +H2O.
+H2O. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$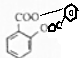 +H2O.
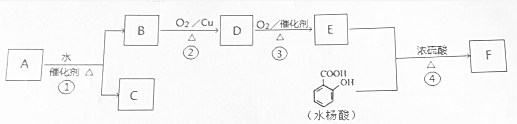
+H2O. 分析 A结构简式为CH2═CH-CH3,含有碳碳双键,在催化剂条件下与水发生加成反应CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH2CH2OH,或CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH(OH)CH3,因B能进行两次氧化生成E,所以B为CH3CH2CH2OH,C为CH3CH(OH)CH3,伯醇在催化剂存在条件下加热与氧气反应生成醛和水,B到D反应方程式为:2CH3CH2CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O,D为CH3CH2CHO,醛氧化成酸,2CH3CH2CHO+O2$→_{△}^{Cu}$2CH3CH2COOH,E为CH3CH2COOH,水杨酸的结构简式为 ,E与水杨酸反应生成F的反应方程为:CH3CH2COOH+
,E与水杨酸反应生成F的反应方程为:CH3CH2COOH+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,结合对应有机物的结构和性质解答该题.
+H2O,结合对应有机物的结构和性质解答该题.
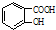
解答 解:(1)水杨酸的结构简式为 ,水杨酸中含氧官能团的名称为羧基、酚羟基,A结构简式为CH2═CH-CH3,含有碳碳双键,在催化剂条件下与水发生加成反应,所以反应①为:CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH2CH2OH,
,水杨酸中含氧官能团的名称为羧基、酚羟基,A结构简式为CH2═CH-CH3,含有碳碳双键,在催化剂条件下与水发生加成反应,所以反应①为:CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH2CH2OH,
故答案为:羧基、酚羟基;加成反应;
(2)A在催化剂条件下与水发生加成反应CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH2CH2OH,或CH2═CH-CH3+H2O $→_{△}^{催化剂}$CH3CH(OH)CH3,因B能进行两次氧化生成E,所以B为CH3CH2CH2OH,C为CH3CH(OH)CH3,
故答案为:CH3CH(OH)CH3;
(3)D为CH3CH2CHO,与银氨溶液反应,乙醛与银氨溶液发生银镜反应,反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$2Ag↓+CH3CH2COONH4+3NH3↑+H2O,
故答案为:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$2Ag↓+CH3CH2COONH4+3NH3↑+H2O;
(4)E为CH3CH2COOH,水杨酸的结构简式为 ,E与水杨酸反应生成F的反应方程为:CH3CH2COOH+
,E与水杨酸反应生成F的反应方程为:CH3CH2COOH+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:CH3CH2COOH+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O;
+H2O;
(5)水杨酸的结构简式为 ,水杨酸中含有-OH和-COOH,可发生酯化反应,两分子之间脱去两分子水形成一种环状化合物为:2
,水杨酸中含有-OH和-COOH,可发生酯化反应,两分子之间脱去两分子水形成一种环状化合物为:2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生判断及知识综合运用能力,明确合成中物质的结构、官能团及反应条件来推断各物质是解答本题的关键,注意体会正逆合成法的综合应用来分析,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体甲可与Z的某种氢化物反应生成强酸 | |
| B. | W元素的晶体单质是一种良好的半导体材料 | |
| C. | X分别与Y,Z,M,W形成的常见化合物中,稳定性最好的是XM | |
| D. | 化合物乙中一定只有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3溶液(BaCl2) | B. | FeCl2溶液(KSCN) | ||
| C. | 海带灰过滤所得的溶液(淀粉溶液) | D. | NaOH溶液(CaCl2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | A酸比B酸的电离程度小 | |
| B. | A是强酸,B是弱酸 | |
| C. | pH=1时,B酸的物质的量浓度比A酸大 | |
| D. | 将pH=1的A酸和B酸稀释成pH=5的溶液,A酸所需加入的水量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 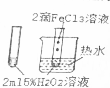 验证FeCl3对H2O2分解反应有催化作用 | |
| B. | 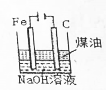 制备Fe(OH)2并能较长时间观察其颜色 | |
| C. |  验证盐酸、碳酸、苯酚酸性的强弱 | |
| D. |  制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离、提纯→确定化学式→确定最简式→确定结构式 | |
| B. | 分离、提纯→确定最简式→确定化学式→确定结构式 | |
| C. | 分离、提纯→确定结构式→确定最简式→确定化学式 | |
| D. | 确定化学式→确定最简式→确定结构式→分离、提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com