
 7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。 2SO3(g) ΔH=—196.6 kJ·mol-1
2SO3(g) ΔH=—196.6 kJ·mol-1 2NO2(g) ΔH=—113.0 kJ·mol-1
2NO2(g) ΔH=—113.0 kJ·mol-1 SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电池充电时,电池负极和电源的负极相连接 |
| B.电池充电时,阴极反应为:Pb - 2e- + SO42-=PbSO4 |
| C.电池放电时,电池负极周围溶液c(H+)不断增大 |
| D.电池放电时,每消耗1mol Pb,共生成1mol PbSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol任何物质都含有6.02×1023个分子 |
| B.0.012 kg12C中含有约6.02×1023个碳原子 |
| C.1 mol水分子中含有2mol氢原子和1mol氧原子 |
| D.1 mol Ne中约含有6.02×1024个电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
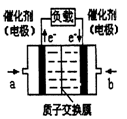
| A.右电极为电池正极,b处通入的物质是氧气 |
| B.左电极为电池负极,a处通入的物质是氧气 |
| C.供电时的总反应为:2H2 + O2 = 2H2O |
| D.H2在负极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ③实验过程中取出盐桥,原电池仍继续工作
③实验过程中取出盐桥,原电池仍继续工作| A.①② | B.②③ | C.②④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO2+4H2O。(已知甲醇的标准燃烧热为-725.76kJ ·mol-1)
2CO2+4H2O。(已知甲醇的标准燃烧热为-725.76kJ ·mol-1)
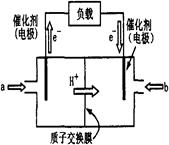
 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数表达式K= ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常K将 (填增大、减小、不变),其反应的正反应速率将 (填增大、减小、不变);逆反应速率将 (填增大、减小、不变);温度升高 (填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数表达式K= ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常K将 (填增大、减小、不变),其反应的正反应速率将 (填增大、减小、不变);逆反应速率将 (填增大、减小、不变);温度升高 (填有利或不利于)电池将化学能转化为电能。 +b kJ·mol-1。若常温下一定量的甲醇完全燃烧生成液态水释放出了1451.52 kJ的能量,则等质量的甲醇利用图示装置理论上可提供 mol电子的电量。
+b kJ·mol-1。若常温下一定量的甲醇完全燃烧生成液态水释放出了1451.52 kJ的能量,则等质量的甲醇利用图示装置理论上可提供 mol电子的电量。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是
体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是 
| A.该电池工作过程中,H+浓度不断增大 |
| B.该电池在高温环境下能提供更好的动力 |
| C.该电池负极反应为:H2—2e—=2H+ |
| D.该电池正极反应为O2+4e—=2O2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com