
| A. | MgCl2+Ca(OH)2═CaCl2+Mg(OH)2↓ | B. | Mg(OH)2+2HCl═MgCl2+2H2O | ||
| C. | Mg(OH)2+H2SO4═MgSO4+2H2O | D. | MgCl2$\frac{\underline{\;通电\;}}{熔融}$Mg+Cl2↑ |
分析 流程分析利用贝壳分解生成氧化钙,溶于水得到氢氧化钙加入到母液中沉淀镁离子,过滤得到氢氧化镁沉淀,加入盐酸溶解富集镁元素,通过浓缩蒸发冷却结晶方法得到氯化镁晶体,氯化氢气流中脱水得到氯化镁固体,电解熔融氯化镁制备镁.
解答 解:从海水中提取镁的工艺流程:利用贝壳分解生成氧化钙CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,溶于水得到氢氧化钙CaO+H2O═Ca(OH)2,加入到母液中沉淀镁离子Mg2++2OH -=Mg(OH)2↓,过滤得到氢氧化镁沉淀,加入盐酸溶解富集镁元素2HCl+Mg(OH)2═MgCl2+2H2O,通过浓缩蒸发冷却结晶方法得到氯化镁晶体,氯化氢气流中脱水得到氯化镁固体,电解熔融氯化镁制备镁MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
A、海水提取镁需要海水中加入氢氧化钙沉淀镁离子,故A不符合;
B、过滤得到的氢氧化镁沉淀中加入盐酸溶解,得到氯化镁溶液,含有此反应,故B不符合;
C、氢氧化镁溶解需要的是盐酸,若加入硫酸会引入杂质离子硫酸根离子,不需此反应,故C符合;
D、电解熔融氯化镁是制备金属镁的方法,有此反应,故D不符合;
故选C.
点评 本题考查元素及其化合物,明确流程中发生的化学反应是解答的关键,注重基础知识和实验基本技能的训练,题目难度中等.


科目:高中化学 来源: 题型:解答题
 实验探究气体的体积与物质的量的关系:
实验探究气体的体积与物质的量的关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:6:1 | B. | 8:6:1 | C. | 3:3:1 | D. | 2:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料表 | 精制海盐.碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(2007)第005号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封.避光.防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
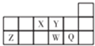
| A. | 离子Y2-和Z3+的核外电子排布相同 | |
| B. | X3-的离子半径小于Z3+的离子半径 | |
| C. | 元素Y的最高正价与最低负价绝对值之和为8 | |
| D. | 元素W的气态氢化物的稳定性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
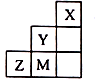
| A. | 离子半径:M->Z2->Y- | |
| B. | 气态氢化物稳定性:Y>Z>M | |
| C. | Z元素形成的氧化物都是共价化合物 | |
| D. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物的水化物的酸性甲比乙强 | |
| B. | 气态氢化物的稳定性甲比乙弱 | |
| C. | 阴离子的还原性甲比乙弱 | |
| D. | 甲的单质比乙的单质更易与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O+H2O?H3O++OH- | B. | Cu(NO3)2═Cu2++NO3- | ||
| C. | H2CO3?2H++CO32- | D. | NaOH?Na++OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com