
ŅŃÖŖ£ŗH2(g)£«F2(g) === 2HF(g) ”÷H£½£270kJ£Æmol£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®1øöĒāĘų·Ö×ÓÓė1øö·śĘų·Ö×Ó·“Ӧɜ³É2øö·ś»ÆĒā·Ö×ӷųö270kJ
B£®1molĒāĘųÓė1mol·śĘų·“Ӧɜ³É2molŅŗĢ¬·ś»ÆĒā·Å³öµÄČČĮæŠ”ÓŚ270kJ
C£®ŌŚĻąĶ¬Ģõ¼žĻĀ£¬1molĒāĘųÓė1mol·śĘųµÄÄÜĮæ×ÜŗĶ“óÓŚ2mol·ś»ÆĒāĘųĢåµÄÄÜĮæ
D£®2mol·ś»ÆĒāĘųĢå·Ö½ā³É1molµÄĒāĘųŗĶ1molµÄ·śĘų·Å³ö270kJČČĮæ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
A£®100 mL 0.1 mol/L K2SO4ČÜŅŗÖŠ£¬ŗ¬ÓŠŃõŌ×ÓŹżĪŖ0.04 NA
B£®100 g 17%µÄ°±Ė®ÖŠ£¬ŗ¬ÓŠ°±·Ö×ÓŹżĪŖNA
C£®1 mol NaÓė×ćĮæO2·“Ó¦£¬Éś³ÉNa2OŗĶNa2O2µÄ»ģŗĻĪļ£¬×ŖŅʵĵē×ÓŹżĪŖNA
D£®25 ”ꏱ£¬1.0 L pH£½13µÄBa(OH)2ČÜŅŗÖŠ£¬ŗ¬ÓŠµÄOH£ŹżÄæĪŖ0.2 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀ±ķŹĒ¼øÖÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£Źż”¢ÄŃČܵē½āÖŹµÄČܶȻżKsp(25 ”ę)”£
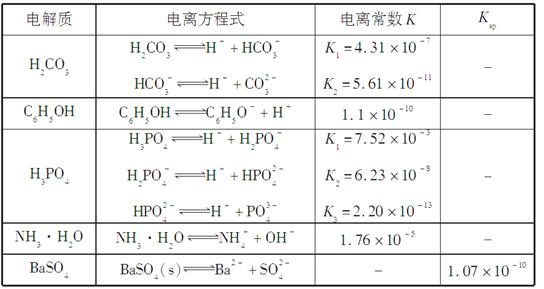
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öC6H5OHÓėNa3PO4·“Ó¦µÄĄė×Ó·½³ĢŹ½______________”£
(2)25 ”ꏱ£¬Ļņ10 mL 0.01 mol”¤L£1 C6H5OHČÜŅŗÖŠµĪ¼ÓV mL 0.01 mol”¤L£1°±Ė®£¬»ģŗĻČÜŅŗÖŠĮ£×ÓÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ________(ĢīŃ”Ļī×ÖÄø)”£
a£®Čō»ģŗĻŅŗpH>7£¬ŌņV”Ż10
b£®V£½5Ź±£¬2c(NH3”¤H2O)£«2c(NH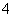 )£½c(C6H5O£)£«c(C6H5OH)
)£½c(C6H5O£)£«c(C6H5OH)
c£®V£½10Ź±£¬»ģŗĻŅŗÖŠĖ®µÄµēĄė³Ģ¶ČŠ”ÓŚ0.01 mol”¤L£1 C6H5OHČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č
d£®Čō»ģŗĻŅŗpH<7£¬Ōņc(NH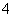 )>c(C6H5O£)>c(H£«)>c(OH£)
)>c(C6H5O£)>c(H£«)>c(OH£)
(3)Ė®½ā·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż³ĘĪŖĖ®½ā³£Źż(ÓĆKh±ķŹ¾)£¬Ąą±Č»ÆŃ§Ę½ŗā³£ŹżµÄ¶ØŅ唣25”ꏱ£¬Na2CO3µŚŅ»²½Ė®½ā·“Ó¦µÄĖ®½ā³£ŹżKh£½________
mol”¤L£1”£
(4)ČēĶ¼ĖłŹ¾£¬ÓŠT1”¢T2²»Ķ¬ĪĀ¶ČĻĀĮ½ĢõBaSO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻß(ŅŃÖŖBaSO4µÄKspĖęĪĀ¶ČÉżø߶ųŌö“ó)”£
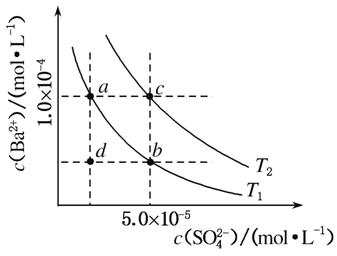
¢ŁT2________25 ”ę(Ģī”°>”±”°<”±»ņ”°£½”±)”£
¢ŚĢÖĀŪT1ĪĀ¶ČŹ±BaSO4µÄ³ĮµķČܽāĘ½ŗāĒśĻߣ¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ________(ĢīŃ”Ļī×ÖÄø)”£
a£®¼ÓČėNa2SO4²»ÄÜŹ¹ČÜŅŗÓÉaµć±äĪŖbµć
b£®ŌŚT1ĒśĻßÉĻ·½ĒųÓņ(²»ŗ¬ĒśĻß)ČĪŅāŅ»µćŹ±£¬¾łÓŠBaSO4³ĮµķÉś³É
c£®Õō·¢ČܼĮæÉÄÜŹ¹ČÜŅŗÓÉdµć±äĪŖĒśĻßÉĻa”¢bÖ®¼äµÄijŅ»µć(²»ŗ¬a”¢b)
d£®ÉżĪĀæÉŹ¹ČÜŅŗÓÉbµć±äĪŖdµć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®±ČĄżÄ£ŠĶ £ŗæÉŅŌ±ķŹ¾¶žŃõ»ÆĢ¼·Ö×Ó£¬Ņ²æÉŅŌ±ķŹ¾Ė®·Ö×Ó
£ŗæÉŅŌ±ķŹ¾¶žŃõ»ÆĢ¼·Ö×Ó£¬Ņ²æÉŅŌ±ķŹ¾Ė®·Ö×Ó
B£®ŹŅĪĀĻĀ£¬½«0£®4mol/L HAČÜŅŗŗĶ0£®2mol/LNaOHČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌ»ģŗĻŹ±ČÜŅŗĢå»żµÄ±ä»Æ£©²āµĆ»ģŗĻČÜŅŗµÄpH=5£¬Ōņ»ģŗĻČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc(H+) =1”Į10-5 mol/L
C£®“æĢ¼ŠĀ²ÄĮĻ”°Ģ¼ÄÉĆ×ÅŻÄ”±£¬ĆæøöÅŻÄŗ¬ÓŠŌ¼4000øöĢ¼Ō×Ó£¬Ö±¾¶Ō¼6µ½9nm£¬ŌŚµĶÓŚ-183”ꏱ£¬ÅŻÄ¾ßÓŠÓĄ¾Ć“ÅŠŌ£¬”°Ģ¼ÄÉĆ×ÅŻÄ”±ÓėŹÆÄ«»„ĪŖĶ¬Ī»ĖŲ
D£®ŅŃÖŖ Ag2CrO4µÄKspĪŖ1.12”Į10£12£¬Ōņ½«µČĢå»żµÄ1”Į10£4 mol”¤L£1µÄAgNO3ČÜŅŗŗĶ
1”Į10£4 mol”¤L£1””K2Cr04ČÜŅŗ»ģŗĻ£¬²»»įÓŠAg2CrO4³Įµķ²śÉś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖČČ»Æѧ·½³ĢŹ½£ŗ
H2O(g)£½H2(g) + 1/2O2(g) ”÷H = +241.8kJ£Æmol
H2(g)+ 1/2O2(g) £½ H2O(1) ”÷H = £285.8kJ£Æmol
µ±1gŅŗĢ¬Ė®±äĪŖĖ®ÕōĘųŹ±£¬ĘäČČĮæ±ä»ÆŹĒ£Ø £©
A£®ĪüČČ88kJ B£® ĪüČČ2.44KJ C£®·ÅČČ44kJ D£® ĪüČČ44KJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĆܱÕČŻĘ÷·¢ÉśĻĀĮŠ·“Ó¦aA(g) cC(g)£«dD(g)£¬·“Ó¦“ļµ½Ę½ŗāŗ󣬽«ĘųĢåĢå»żŃ¹Ėõµ½ŌĄ“µÄŅ»°ė£¬µ±ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬DµÄÅضČĪŖŌĘ½ŗāµÄ1.8±¶£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
cC(g)£«dD(g)£¬·“Ó¦“ļµ½Ę½ŗāŗ󣬽«ĘųĢåĢå»żŃ¹Ėõµ½ŌĄ“µÄŅ»°ė£¬µ±ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬DµÄÅضČĪŖŌĘ½ŗāµÄ1.8±¶£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A£®AµÄ×Ŗ»ÆĀŹ±ä“ó B£®Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
C£®DµÄĢå»ż·ÖŹż±ä“ó D£®a £¼ c£«d
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Ōö“ó·“Ó¦ĪļÅØ¶Č£¬æÉŌö“óµ„Ī»Ģå»żÄŚ»ī»Æ·Ö×ӵİŁ·ÖŹż£¬“Ó¶ųŹ¹ÓŠŠ§Åöײ“ĪŹżŌö“ó
B£®ÓŠĘųĢå²Ī¼ÓµÄ»Æѧ·“Ó¦£¬ČōŌö“óŃ¹Ēæ£Ø¼“ĖõŠ”·“ӦȯĘ÷µÄĢå»ż£©£¬æÉŌö¼Ó»ī»Æ·Ö×ӵİŁ·ÖŹż£¬“Ó¶ųŹ¹·“Ó¦ĖŁĀŹŌö“ó
C£®ÉżøßĪĀ¶ČÄÜŹ¹»Æѧ·“Ó¦ĖŁĀŹŌö“ó£¬ŌŅņŹĒŌö¼ÓĮĖ·“Ó¦Īļ·Ö×ÓÖŠ»ī»Æ·Ö×ӵİŁ·ÖŹż
D£®“߻ƼĮ²»Ó°Ļģ·“Ó¦»ī»ÆÄܵ«ÄÜŌö“óµ„Ī»Ģå»żÄŚ»ī»Æ·Ö×Ó°Ł·ÖŹż£¬“Ó¶ųŌö“ó·“Ó¦ĖŁĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·“Ó¦ÖŠ£¬²»ŹōÓŚĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶ£¬µ«ŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ
A. 2Na + 2H2O ==2NaOH + H2ӟ B. CH4 + 2O2==CO2 + 2H2O
C. KClO3==2KCl + 3O2ӟ D. CaCO3 + 2HCl == CaCl2 + H2O + CO2ӟ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ»¹ŌŠŌ£ŗHSO >I££¬Ńõ»ÆŠŌ£ŗIO
>I££¬Ńõ»ÆŠŌ£ŗIO >I2”£
>I2ӣ
(1)ŌŚNaIO3ČÜŅŗÖŠµĪ¼ÓÉŁĮæNaHSO3ČÜŅŗ£¬·¢ÉśĻĀĮŠ·“Ó¦”£ÅäĘ½·“Ó¦·½³ĢŹ½£¬²¢±ź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣
”õNaIO3£«”õNaHSO3ØD”ś”õI2£«”õNa2SO4£«”õH2SO4£«”õH2O
(2)ŌŚNaIO3ČÜŅŗÖŠµĪ¼Ó¹żĮæNaHSO3ČÜŅŗ£¬·“Ó¦ĶźČ«£¬ĶĘ²ā·“Ó¦ŗóČÜŅŗÖŠµÄ»¹Ō²śĪļĪŖ________________(Ģī»ÆѧŹ½)”£
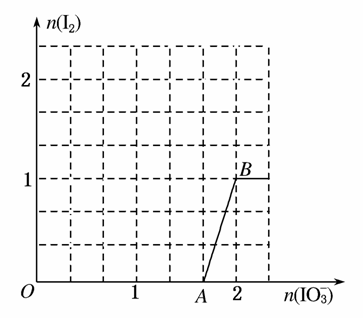
(3)ŌŚŗ¬5 mol NaHSO3µÄČÜŅŗÖŠÖšµĪ¼ÓČėNaIO3ČÜŅŗ£¬¼ÓČėNaIO3µÄĪļÖŹµÄĮæŗĶĪö³öI2µÄĪļÖŹµÄĮæµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾”£Š“³ö·“Ó¦¹ż³ĢÖŠÓėAB¶ĪĒśĻ߶ŌÓ¦µÄĄė×Ó·½³ĢŹ½____________£»µ±ČÜŅŗÖŠI£ÓėI2µÄĪļÖŹµÄĮæÖ®±ČĪŖ53Ź±£¬¼ÓČėµÄNaIO3ĪŖ________ mol”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com