
·ÖĪö £Ø1£©øƶžŌŖĖįµŚŅ»²½ĶźČ«µēĄė£¬µŚ¶ž²½²æ·ÖµēĄė£¬ĖµĆ÷A2-ÄÜĖ®½ā”¢HA-Ö»µēĄė²»Ė®½ā£¬Na2AĖ®ČÜŅŗÖŠA2-Ė®½āµ¼ÖĀČÜŅŗ³Ź¼īŠŌ£»
£Ø2£©£Ø2£©øł¾ŻµēĄė·½³ĢŹ½ÖŖ£¬HA-Ö»µēĄė²»Ė®½ā£¬0.1mol•L-1NaHAČÜŅŗµÄpH=2£¬ŌņHA-µēĄė³öĒāĄė×ÓÅضČĪŖ0.01mol/L£¬H2AµŚŅ»²½µēĄė³öµÄĒāĄė×ÓŅÖÖʵŚ¶ž²½µēĄė£®
½ā“š ½ā£ŗ£Ø1£©øƶžŌŖĖįµŚŅ»²½ĶźČ«µēĄė£¬µŚ¶ž²½²æ·ÖµēĄė£¬ĖµĆ÷A2-ÄÜĖ®½ā”¢HA-Ö»µēĄė²»Ė®½ā£¬Na2AĖ®ČÜŅŗÖŠA2-Ė®½āµ¼ÖĀČÜŅŗ³Ź¼īŠŌ£¬Ė®½ā·½³ĢŹ½ĪŖA2-+H2O?HA-+OH-£¬¹Ź“š°øĪŖ£ŗ¼īŠŌ£»A2-+H2O?HA-+OH-£»
£Ø2£©øł¾ŻµēĄė·½³ĢŹ½ÖŖ£¬HA-Ö»µēĄė²»Ė®½ā£¬0.1mol•L-1NaHAČÜŅŗµÄpH=2£¬ŌņHA-µēĄė³öĒāĄė×ÓÅضČĪŖ0.01mol/L£¬H2AµŚŅ»²½ĶźČ«µēĄėÉś³É0.1mol/LµÄĒāĄė×Ó£¬µŚŅ»²½µēĄė³öµÄĒāĄė×ÓŅÖÖʵŚ¶ž²½µēĄė£¬ĖłŅŌµŚ¶ž²½µēĄė³öµÄĒāĄė×ÓÅØ¶ČŠ”ÓŚ0.01mol/L£¬ŌņH2AČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæÅضČÓ¦Š”ÓŚ0.11mol/L£¬
¹Ź“š°øĪŖ£ŗ£¼£»HA-²æ·ÖµēĄėĒŅH2AµŚŅ»²½µēĄė³öµÄĒāĄė×ÓŅÖÖʵŚ¶ž²½µēĄė£®
µćĘĄ ±¾Ģāæ¼²éČõµē½āÖŹµÄµēĄėŗĶŃĪµÄĖ®½ā£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāĢāøÉŠÅĻ¢ÖŠH2AµÄĮ½²½µēĄė²»Ķ¬£¬µŚŅ»²½ĶźČ«µēĄė”¢µŚ¶ž²½²æ·ÖµēĄė£¬µ¼ÖĀHA-Ö»µēĄė²»Ė®½ā£¬ĪŖŅדķĢā£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£®


 Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCNČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬µēĄė¶Č±£³Ö²»±ä£¬$\frac{c£Ø{F}^{-}£©}{c£ØHF£©}$Ōö“ó | |
| B£® | Ļņ°±Ė®ÖŠ¼ÓČėNH4Cl¹ĢĢ壬ČÜŅŗÖŠ$\frac{c£ØN{H}_{3}•{H}_{2}O£©•c£Ø{H}^{+}£©}{c£ØN{{H}_{4}}^{+}£©}$Ōö“ó | |
| C£® | NH4HCO3ČÜŅŗ³Ź¼īŠŌ£¬ÓÉ“ĖæÉÖŖKb£ØNH3•H2O£©£¾Ka1£ØH2CO3£© | |
| D£® | AgClŌŚ±„ŗĶNaClČÜŅŗÖŠµÄČܽā¶Č¼°Ksp¶¼±ČŌŚ“æĖ®ÖŠµÄŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
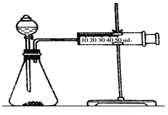 Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲŗܶą£¬Ä³æĪĶāŠĖȤŠ”×éÓĆŹµŃéµÄ·½·Ø½ųŠŠĢ½¾æ£®
Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲŗܶą£¬Ä³æĪĶāŠĖȤŠ”×éÓĆŹµŃéµÄ·½·Ø½ųŠŠĢ½¾æ£®| ŹµŃé²½Öč | ĻÖĻó | ½įĀŪ |
| ¢Ł·Ö±šČ”µČĢå»żµÄ2mol/LµÄĮņĖįÓŚŹŌ¹ÜÖŠ£»¢Ś·Ö±šĶ¶Čė“óŠ””¢ŠĪדĻąĶ¬µÄAl”¢Fe”¢Mg | ·“Ó¦æģĀż£ŗMg£¾Al£¾Fe | ·“Ó¦ĪļµÄŠŌÖŹŌ½»īĘĆ£¬·“Ó¦ĖŁĀŹŌ½æģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ×鱚 | ĪĀ¶Č | KIČÜŅŗ | H2SO4ČÜŅŗ | µķ·ŪČÜŅŗ | ŹµŃéÄæµÄ | ||
| C£ØKI£© | V | C£ØH2SO4£© | V | ||||
| 1 | 25”ę | 1mol/L | 5mL | 0.1mol/L | 5mL | 3µĪ | l×éŗĶ2×éĢ½¾æ¢ŚĪĀ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£»2×éŗĶ3×éĢ½¾æ·“Ó¦ĪļÅØ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ |
| 2 | 35”ę | 1mol/L | 5mL | 0.1mol/L | 5mL | 3µĪ | |
| 3 | 35”ę | 1mol/L | 5mL | ¢Ł0.2mol/LĮņĖį | 5mL | 3µĪ | |
| ŹµŃé·½°ø | Ō¤ĘŚŹµŃéĻÖĻóÓė½įĀŪ |
| ȔɣĮæµāĖ®ÓŚŹŌ¹ÜÖŠ£¬µĪČė¼øµĪµķ·ŪČÜŅŗ£¬Č»ŗóÖšµĪ¼ÓČė1mol/L KOHČÜŅŗ£¬¹Ū²ģĻÖĻó£® | ČōĄ¶É«²»ĶŹÉ«£¬Ōņ¼ŁÉč¶žÕżČ·£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Éś»īÖŠŹ¹ÓƵÄĘÆ°×·ŪŗĶ·ŹŌķ¶¼ŹĒ»ģŗĻĪļ | |
| B£® | ŃĢ”¢Īķ”¢¶¹½¬”¢ÓŠÉ«²£Į§¶¼ŹĒ½ŗĢå | |
| C£® | ĘūÓĶŹōÓŚ»ģŗĻĪļ£¬¶ųŅŗĀČ”¢±ł“×Ėį¾łŹōÓŚ“æ¾»Īļ | |
| D£® | ÕįĢĒ”¢ĻõĖį¼ŲŗĶĮņĖį±µ·Ö±šŹōÓŚ·Ēµē½āÖŹ”¢Ēæµē½āÖŹŗĶČõµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéµÄµē×ÓŹ½£ŗ | B£® | CCl4·Ö×ӵıȥżÄ£ŠĶ£ŗ | ||
| C£® | ŅŅĻ©Óė¶”¶žĻ©µÄ×ī¼ņŹ½ĻąĶ¬ | D£® | 2-¼×»ł¶”“¼µÄ½į¹¹¼ņŹ½£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol/LµÄ“×ĖįČÜŅŗÖŠc£ØH+£©=0.01 mol/L | |
| B£® | “×ĖįÄÜÓėĖ®ŅŌČĪŗĪ±ČĄż»„ČÜ | |
| C£® | 10mL1mol/L“×ĖįĒ”ŗĆÓė10mL1mol/LNaOHČÜŅŗĶźČ«·“Ó¦ | |
| D£® | “×ĖįČÜŅŗµÄµ¼µēŠŌ±ČŃĪĖįµÄČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢģČ»Ęų”¢¾Ę¾«·Ö±šŹōÓŚ»ÆŹÆÄÜŌ“”¢æÉŌŁÉśÄÜŌ“ | |
| B£® | ½šŹōŌŚ³±ŹŖæÕĘųÖŠÉśŠā£¬Ö÷ŅŖŹĒ·¢ÉśĪöĒāøÆŹ“ | |
| C£® | NaClO¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉ×÷ÖÆĪļĘÆ°×¼Į | |
| D£® | øß“æ¹č¹ć·ŗÓ¦ÓĆÓŚĢ«ŃōÄܵē³ŲŗĶ°ėµ¼Ģå²ÄĮĻµÄÖĘŌģ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com