
| 化学式 | 电离常数(25℃) |
| CH3COOH | Ki=1.7×10-5 |
| HClO | Ki=3.0×10-8 |
| H2CO3 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | H2CO3、HCO3-、CH3COO-、ClO- | B. | HClO、HCO3-、CH3COO-、ClO- | ||
| C. | HClO、HCO3-、ClO-、CO32- | D. | HCO3-、CH3COO-、ClO-、CO32- |
分析 根据表中电离平衡常数可知,酸性大小为:CH3COOH>H2CO3>HClO>HCO3-,
A.碳酸的酸性大于HClO,二者能够反应生成碳酸氢根离子和HClO;
B.四种粒子之间不发生反应,能够共存;
C.HClO的酸性大于HCO3-,HClO与碳酸根离子反应生成碳酸氢根离子;
D.四种粒子之间不发生反应,可以共存.
解答 解:根据表中电离平衡常数可知,酸性大小为:CH3COOH>H2CO3>HClO>HCO3-,
A.H2CO3的酸性大于HClO,H2CO3、CN-能够反应生成HCO3-和HCN,在溶液中不能大量共存,故A错误;
B.HClO、HCO3-、CH3COO-、ClO-之间不反应,在溶液中能够大量共存,故B正确;
C.HClO的酸性大于HCO3-,HClO与CO32-反应生成HCO3-,在溶液中不能大量共存,故C错误;
D.HCO3-、CH3COO-、ClO-、CO32-之间不反应,在溶液中能够大量共存,故D正确;
故选BD.
点评 本题考查粒子共存的判断,题目难度中等,根据表中数据正确判断酸性强弱为解答关键,注意明确酸性强弱与电离平衡常数的关系,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 液化石油气(LPG)的主要成份是碳氢化合物 | |
| B. | 光化学烟雾是氮氧化物和烃的排放引发的环境污染 | |
| C. | CHCl3不存在同分异构体,可以证明甲烷是以碳原子为中心的正四面体结构 | |
| D. | 甲烷与二氧化碳一样,也是一种温室气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH≡CH | C. | CH2=CHCl | D. | CH≡CCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
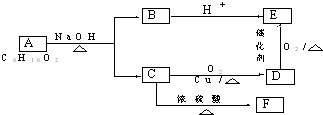
 .
.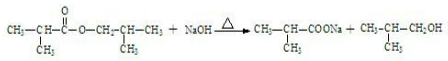 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制氯化铁溶液时,加入少量稀盐酸 | |
| B. | 配制氯化亚铁溶液时,加入少量铁屑 | |
| C. | 在含有酚酞的氨水中加入少量NH4Cl,溶液颜色会变浅 | |
| D. | 在硫酸铜饱和溶液中加入一块胆矾,晶体外形变规则 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
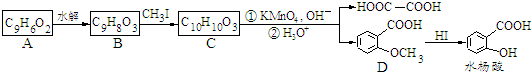
 .
.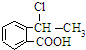 合成
合成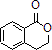 ,写出相关化学反应方程式
,写出相关化学反应方程式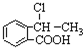 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +H2O+NaCl、
+H2O+NaCl、 +HBr$\stackrel{过氧化物}{→}$
+HBr$\stackrel{过氧化物}{→}$ 、
、 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$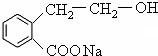 ++NaBr+H2O、2
++NaBr+H2O、2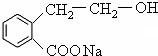 +H2SO4$\stackrel{△}{→}$2
+H2SO4$\stackrel{△}{→}$2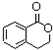 +2H2O+Na2SO4.
+2H2O+Na2SO4.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

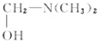 .
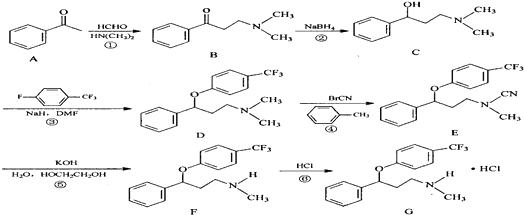
.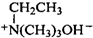 $\stackrel{△}{→}$CH2=CH2;请写出以
$\stackrel{△}{→}$CH2=CH2;请写出以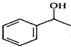 、HCHO、HN(CH3)2为有机原料,合成
、HCHO、HN(CH3)2为有机原料,合成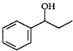 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH}$ CH3CH2OH.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH}$ CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在常温下不溶于浓硝酸,说明铁与浓硝酸不反应 | |
| B. | 将氯气溶于水后溶液呈浅黄绿色,说明氯气与水没有完全反应 | |
| C. | 将某气体通入品红溶液中溶液褪色,说明该气体一定是二氧化硫 | |
| D. | 向溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,说明该溶液中一定有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com