
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-===Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A、①②
B、②③
C、②④
D、③④
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) △H 1 = +489.0 kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= ▲ 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图10所示,则该反应的ΔH ▲ 0(填“>”、“<”或“=”)。


图10 图11
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图11所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ ▲ KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 ▲ 。当氨碳比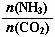 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
▲ 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有 X和
X和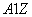 X+两种粒子,下列叙述正确的是
X+两种粒子,下列叙述正确的是
A.一定都是由质子、中子、电子组成的
B.化学性质几乎完全相同
C.质子数一定相等,质量数和中子数一定不相等
D.核电荷数和核外电子数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为
 ,其不可能发生的反应有( )
,其不可能发生的反应有( )
①加成反应 ②取代反应 ③消去反应 ④氧化反应
⑤水解反应 ⑥与氢氧化钠的反应 ⑦与稀盐酸的反应
A.②③④ B.①④⑥
C.③⑤⑦ D.⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
白藜芦醇属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用。某课题组提出了如下合成路线:

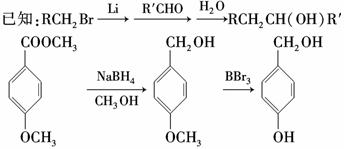
根据以上信息回答下列问题:
(1)白藜芦醇的分子式是____________。
(2)C→D的反应类型是____________;E→F的反应类型是____________。
(3)化合物 A 不与 FeCl3 溶液发生显色反应,能与 NaHCO3反应放出 CO2,推测其核磁共振氢谱(1H-NMR)中显示有________种不同化学环境的氢原子,其个数比为________。
(4)写出A→B 反应的化学方程式:______________________________________。
(5)写出化合物 D、E 的结构简式:D________________________________________,
E__________________。
(6)化合物 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
________________________________________________________________________。
①能发生银镜反应;②含苯环且苯环上只有两种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
在生物体中,细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,则下列有关判断正确的是( )
A、正极的电极反应可能是:
B、负极的电极反应可能是:
C、正极反应主要是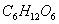 生成
生成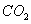 或
或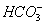
D、负极反应主要是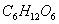 生成
生成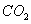 或
或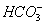
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,我国拥有完全自主产权的氢氧燃料电池车在广州亚运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A、正极反应式为:O2+2H2O+4e-===4OH-
B、工作一段时间后,电解液中KOH的物质的量不变
C、该燃料电池的总反应方程式为:2H2+O2===2H2O
D、用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
M、N、P、E四种金属,①M+N2+====N+M2+ ②M、P用导线连接放入硫酸氢钠溶液中,M表示有大量气泡 ③N、E用导线连接放入E的硫酸溶液中,电极反应为E2++2e-====E,N-2e-====N2+。四种金属的还原性由强到弱顺序是( )
A.PMNE B.ENMP C.PNME D.EPMN
查看答案和解析>>
科目:高中化学 来源: 题型:
月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为________。
(2)Na的原子结构示意图为________,Na在氧气中完全燃烧所得产物的电子式为________。
(3)MgCl在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________(填“高”或“低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为__________________________;SiO2的晶体类型为________。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为________________(写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg 3He,同时可得6000 kg H2和700 kg N2,若以所得H2和N2为原料经一系列反应最多可生产碳酸氢铵________kg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com