
| A. | 14g乙烯和丙烯的混合气体中含有H原子数为2NA | |
| B. | 标准状况下2.24L乙醇与足量Na反应生成H2分子数0.05NA | |
| C. | 每摩尔-CH3中含10NA个电子 | |
| D. | 每摩尔甲苯中含有的碳碳单键的数目为7 NA |
分析 A.乙烯和丙烯的最简式为CH2,根据最简式计算出混合物中含有的氢原子数目;
B.标况下,乙醇为液体,不能使用标况下的气体摩尔体积计算乙醇的物质的量;
C.甲基中含有9个电子,1mol甲基中含有9mol电子;
D.甲苯分子中,苯环中不含碳碳单键,其分子中含有1个碳碳单键.
解答 解:A.14g乙烯和丙烯的混合物中含有1mol最简式CH2,含有2mol氢原子,含有H原子数为2NA,故A正确;
B.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算2.24L乙醇的物质的量,故B错误;
C.甲基中含有9个电子,则每摩尔-CH3中含有9mol电子,含9NA个电子,故C错误;
D.甲苯分子中含有1个碳碳单键,1mol甲苯中含有1mol碳碳单键,含有的碳碳单键的数目为NA,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下乙醇、三氧化硫、水等的状态不是气体,选项C为易错点,注意甲基与甲烷、羟基与氢氧根离子的区别.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 16 | C. | 20 | D. | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
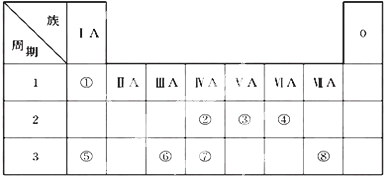
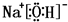 或
或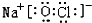 .
.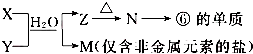
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |  |  |  |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

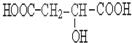 请回答:
请回答: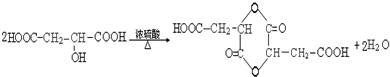 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将锌片换成等量的锌粉 | B. | 加入数滴氯化铜溶液 | ||
| C. | 升高温度 | D. | 加入适量的6mol•L-1的硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.| 引起误差的一些错误操作 | 对CB的影响 |
| 定容时,俯视刻度线 | 偏大 |
| 转移溶液时,玻璃棒下端靠在容量瓶刻度线以上 | 偏小 |
| 洗涤量取浓溶液的量筒并将洗涤液转移到容量瓶 | 偏大 |
| 定容后,经振荡、摇匀、静置、液面低于刻度线再加水 | 偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含有Fe2+、Cu2+、Cl- | |
| B. | c(Fe2-):c(Cu2+)=1:2 | |
| C. | c(Cl-)=6.0mol.L-1,c(Fe2+)=1.2mol.L-1 | |
| D. | c(Fe2+):c(Fe3+)=3:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com