
分析 (1)钠和水反应生成氢氧化钠和氢气,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气;
(2)钠性质活泼,应用沙土扑灭,过氧化钠与水反应生成氢氧化钠和氧气;
(3)一般用弱碱和硫酸铝反应制备氢氧化铝,因氢氧化铝为两性氢氧化物,与强碱反应.
解答 解:(1)钠和水反应生成氢氧化钠和氢气,反应的方程式为2Na+2H2O=2NaOH+H2↑,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)钠性质活泼,与水、氧气反应,应用沙土扑灭,过氧化钠与水反应生成氢氧化钠和氧气,反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:沙土;2Na2O2+2H2O=4Na++4OH-+O2↑;
(3)因氢氧化铝为两性氢氧化物,与强碱反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,一般用弱碱和硫酸铝反应制备氢氧化铝,氨水与硫酸铝反应生成硫酸铵和氢氧化铝,反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+; Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查元素化合物知识,为高考常见题型,把握发生的化学反应为解答的关键,注重基础知识的考查,注意离子反应的书写方法,题目难度不大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:填空题
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_____________________。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
已知:H2(g)+Cl2(g)=2HCl(g)△H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=_____________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
2Cu(s)+ O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,
O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,
C(s)+ O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,
O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,
2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____________。
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图:

①请计算每生成1molNH3放出热量为:_________.
②若起始时向容器内放入1molN2和3molH2达平衡后N2的为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol | B. | 1.0 mol | C. | 2.0 mol | D. | 4.0 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下:
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下: .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
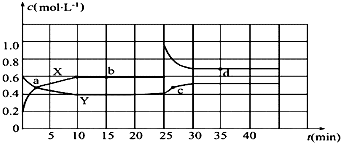
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标准状况下,22.4L氩气含有原子数为2Na | |
| C. | 常温常压下,32g O2和O3混合气所含氧原子数是2NA | |
| D. | 物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数为1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com