
���� ��1����Ӧ�жϼ�ʱ���յ��������γɻ�ѧ��ʱ�ų��������ߣ���Ӧ�����ȷ�Ӧ��
��2����Ԫ�ػ��ϼ�Ϊ+2�ۣ�û�дﵽ��ۣ��ʿ�����ԭ�������������ȼ��ȣ�
��3��Na2S+H2O+SO2��Na2SO3+H2S ����i��
2H2S+SO2��3S+2H2O ����ii��
S+Na2SO3$\stackrel{��}{��}$Na2S2O3 ����iii��2��i+ii+iii�����ܷ�Ӧ����ʽ���ݴ˽��з��������淴Ӧ���ص��Ƿ�Ӧ�ﲻ����ȫת��Ϊ�����
��4����Na2S2O3�����ֽ���������
��� �⣺��1����Ӧ�жϼ�ʱ���յ��������γɻ�ѧ��ʱ�ų��������ߣ���Ӧ�����ȷ�Ӧ���ʷ�Ӧ����ѻ�ѧ�������յ������������������γɻ�ѧ�����ų�����������
�ʴ�Ϊ�����ڣ�
��2��Na2S2O3���л�ԭ�ԣ��ж������ǣ���Ԫ�ػ��ϼ�Ϊ+2�ۣ�û�дﵽ��ۣ����������ȼ��ȣ�
�ʴ�Ϊ����Ԫ�ػ��ϼ�Ϊ+2�ۣ�û�дﵽ��ۣ����������ȼ���
��3��Na2S+H2O+SO2��Na2SO3+H2S ����i��
2H2S+SO2��3S+2H2O ����ii��
S+Na2SO3$\stackrel{��}{��}$Na2S2O3 ����iii��2��i+ii+iii�����ܷ�Ӧ����ʽΪ2Na2S+Na2SO3+3SO2��3Na2S2O3�����淴Ӧ���ص��Ƿ�Ӧ�ﲻ����ȫת��Ϊ�������Ӧ�����Ӧ������ʣ�࣬��˵���ù����д���
���淴Ӧ��
�ʴ�Ϊ��2Na2S+Na2SO3+3SO2��3Na2S2O3�����淴Ӧ��
��4����SO2��������Һ�����ԣ�Na2S2O3�����ֽ⣬��������ͨ���SO2���ܹ�����
�ʴ�Ϊ��SO2��������Һ�����ԣ�Na2S2O3�����ֽ⣮
���� ���⿼�����ȷ�Ӧ��ע�����շ�Ӧ�����ʱ�Ĺ�ϵ���Լ�����ʽ����д�����淴Ӧ���ص�ȣ������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
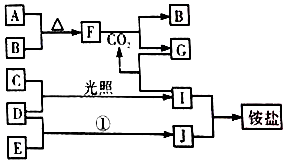 ��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ��ʣ����ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ����Ҫ�̵���Ӧ
��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ��ʣ����ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ����Ҫ�̵���Ӧ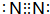 ��F
��F ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7.8gNa2O2�к������ӵ���ĿΪ0.1NA | |
| B�� | 25��ʱ��1L pH=1��H2SO4��Һ�к�H+����ĿΪ0.2NA | |
| C�� | 9.0g���ۺ������ǵĻ�����к�̼ԭ�ӵ���ĿΪ0.3NA | |
| D�� | ��10mL 1mol/L FeCl3��Һ�����ˮ�У���������������������ĿΪ0.01NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��ؿɽ�����ת��Ϊ��ѧ�� | |
| B�� | ��ѧ��Ӧһ�������������仯 | |
| C�� | ȼ��ȼ���ܽ���ѧ��ת��Ϊ���� | |
| D�� | ֲ��Ĺ�����ý�̫����ת��Ϊ��ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ����1 molCl2��������ˮ�У�HClO��Cl-��C1O-������֮��Ϊ2NA | |
| B�� | ��״���£�22.4L NH3��HCl�Ļ�������к��еķ�������ΪNA | |
| C�� | �����£�pH=2��H2SO4��Һ�к��е�H+��ĿΪ0.02NA | |
| D�� | �����£�0.3mol Fe��������ˮ������ȫ��Ӧʧȥ�ĵ�����Ϊ0.8NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ��A1��OH��3����ı����������ܷ���������ЧӦ | |
| B�� | ��ά�غ;�����ϩ��Ϊ�ɽ���ĸ߷��ӻ����� | |
| C�� | ˮ�������Ͳ����������ڹ����β�Ʒ | |
| D�� | ��ʴ�Ͻ�ķ���ԭ����绯ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
 | 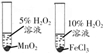 |  |  |
| ȷ��ȡһ�����KMnO4�� ��Һ | ̽����ͬ�����Է�Ӧ���ʵ�Ӱ�� | �۲�Fe��OH��2����ɫ | ֤���ǽ�����S��Si |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na2O2+2H218O�T4NaOH+18O2�� | |
| B�� | K37ClO3+6HCl�TK37Cl+3Cl2��+3H2O | |
| C�� | NH4Cl+2H2O?NH3•2H2O+HCl | |
| D�� | CH3COOH+CH3CH218OH$?_{��}^{Ũ����}$CH3CO18OCH2CH3+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com