
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O
+3H2O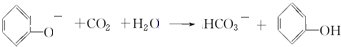 .
. 分析 ①在浓硫酸作催化剂、加热条件下,甲苯和硝酸发生取代反应生成TNT;
②乙醛与银氨溶液反应生成醋酸铵、银单质、氨气和水;
③2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水;
④一定条件下,乙烯和水发生加成反应生成乙醇;
⑤苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠.
解答 解:①浓硫酸作催化剂、加热条件下,甲苯和硝酸发生取代反应生成TNT,反应为 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O,
+3H2O,
故答案为: +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O;
+3H2O;
②乙醛与银氨溶液发生银镜反应,反应的化学方程式为:CH3CHO+2[Ag(NH3)2]OH$\stackrel{水浴加热}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O,故答案为:CH3CHO+2[Ag(NH3)2]OH$\stackrel{水浴加热}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O;
③2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水,反应的化学方程式为:CH3CHBrCH3+NaOH $→_{△}^{乙醇}$CH3-CH=CH2↑+NaBr+H2O,
故答案为:CH3CHBrCH3+NaOH $→_{△}^{乙醇}$CH3-CH=CH2↑+NaBr+H2O;
④一定条件下,乙烯和水发生加成反应生成乙醇,反应方程式为CH2=CH2+H2O$\stackrel{一定条件下}{→}$CH3CH2OH,故答案为:CH2=CH2+H2O$\stackrel{一定条件下}{→}$CH3CH2OH;
⑤苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠,反应的化学方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,离子反应方程式为: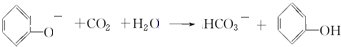 ,故答案为:
,故答案为: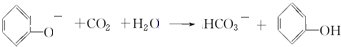 .
.
点评 本题考查化学方程式有关书写,为高频考点,明确物质官能团及其性质关系、反应条件及产物是解本题关键,注意苯酚钠和二氧化碳、水反应生成碳酸氢钠而不是碳酸钠,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 第一周期第ⅠA族 | B. | 第二周期第VⅡA族 | C. | 第三周期第VⅡA族 | D. | 第三周期第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 全对 | B. | 全错 | C. | ③⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com