
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
分析 (1)温度越高,反应速率越快;
(2)为使滤液中的Fe2+完全被H2O2氧化,加入的氧化剂要过量,且使反应物充分反应;
(3)氢氧根离子和铁离子反应生成红褐色沉淀氢氧化铁;
(4)白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算;
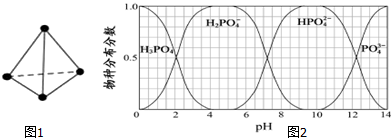
(5)根据为获得尽可能纯的NaH2PO4,pH应控制从图表中找出H2PO4-分布分数最大值所在区间;溶液中主要含磷物种浓度大小关系可由图表得出.
解答 解:(1)温度越高,反应速率越快,所以反应加热的目的是加快铁与稀硫酸反应速率,
故答案为:加快Fe和稀硫酸的反应速率;
(2)A、加热,使反应在较高温度下进行,虽然反应速率加快,但能促进亚铁离子水解而产生杂质,故错误;
B、用氨水调节溶液pH=7,亚铁离子和氢氧根离子反应生成氢氧化亚铁杂质,故错误;
C、加入适当过量的H2O2溶液,导致铁离子能完全反应,故正确;
D、缓慢滴加H2O2溶液并搅拌,反应物接触面积增大,能使铁离子完全反应,故正确;
故选CD;
(3)碱性条件下,溶液中含有大量氢氧根离子,氢氧根离子和铁离子反应生成红褐色沉淀氢氧化铁,导致反应得到的FePO4•H2O固体呈棕黄色,
故答案为:Fe(OH)3;
(4)已知白磷固体(P4 结构如图1所示)的燃烧热为.2378.0kJ/mol,反应的热化学方程式为:P4(s)+5O2(g)=P4O10 (s)△H=-2378.0 kJ/mol,白磷燃烧的方程式为P4+5O2=P4O10,1mol白磷完全燃烧需拆开6mol P-P、5mol O=O,形成12molP-O、4mol P=O,所以12mol×360kJ/mol+4mol×xkJ/mol-(6mol×197 kJ/mol+5 mol×499 kJ/mol)=2378.0kJ,x=433.75≈434.
故答案为:-2378.0;434;
(5)为获得尽可能纯的NaH2PO4,pH应控制从图表中找出H2PO4-分布分数最大值所在区间,即4~5.5(介于此区间内的任意值或区间均可),溶液中主要含磷物种浓:度大小关系可由图表得出 c(HPO42-)>c(H2PO4-),
故答案为:4~5.5(介于此区间内的任意值或区间均可);c(HPO42-)>c(H2PO4-).
点评 本题以铁及其化合物为载体考查了物质的制备,涉及氧化还原反应、实验操作、反应速率的影响因素等知识点,根据物质之间的关系式、实验操作的规范性、影响反应速率的因素等知识点来分析解答,题目难度中等.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. 的沸点高.(填高或低)
的沸点高.(填高或低)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.0176 | B. | 0.1600 | C. | 0.1200 | D. | 0.2400 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
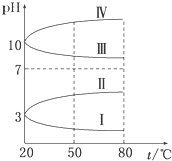 NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④②①③ | B. | ①④③② | C. | ②③①④ | D. | ②④①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
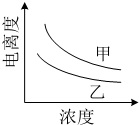 结合下表回答下列问题(均为25℃时的数据)
结合下表回答下列问题(均为25℃时的数据)| 酸 | 电离平衡常数(Ka) | 酸 | 电离平衡常数(Ka) |
| CH3COOH | 1.7×10-5 | H3BO3 | 5.8×10-10 |
| H2CO3 | Ka1=4.2×10-7 Ka2=5.6×10-11 | HNO2 | 7.1×10-4 |
| HCN | 6.2×10-10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com