
 +H2O;
+H2O; .合成路线示例如下:
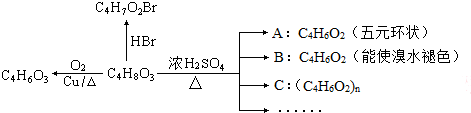
.合成路线示例如下:分析 化合物C4H8O3与Na2CO3溶液反应放出CO2,说明有羧基,C4H8O3与溴化氢发生取代反应生成C4H7O2Br,能被氧气氧化得C4H6O3,说明有羟基,C4H8O3在浓硫酸的作用下发生酯化反应生成五元环A,根据A的分子式可知,C4H8O3为CH2OHCH2CH2COOH,C4H8O3在浓硫酸的作用下发生消去反应生成B为CH2=CHCH2COOH,C4H8O3在浓硫酸的作用下发生缩聚反应生成C为 ,以乙烯和CH2OHCH2CH2COOH为原料制备化合物CH3CH2OOCCH2CH2COOCH2CH3,可以先将CH2OHCH2CH2COOH经过两步氧化得HOOCCH2CH2COOH,乙烯水化得乙醇,乙醇与HOOCCH2CH2COOH发生酯化得CH3CH2OOCCH2CH2COOCH2CH3,以此解答该题.
,以乙烯和CH2OHCH2CH2COOH为原料制备化合物CH3CH2OOCCH2CH2COOCH2CH3,可以先将CH2OHCH2CH2COOH经过两步氧化得HOOCCH2CH2COOH,乙烯水化得乙醇,乙醇与HOOCCH2CH2COOH发生酯化得CH3CH2OOCCH2CH2COOCH2CH3,以此解答该题.
解答 解:化合物C4H8O3与Na2CO3溶液反应放出CO2,说明有羧基,C4H8O3与溴化氢发生取代反应生成C4H7O2Br,能被氧气氧化得C4H6O3,说明有羟基,C4H8O3在浓硫酸的作用下发生酯化反应生成五元环A,根据A的分子式可知,C4H8O3为CH2OHCH2CH2COOH,C4H8O3在浓硫酸的作用下发生消去反应生成B为CH2=CHCH2COOH,C4H8O3在浓硫酸的作用下发生缩聚反应生成C为 ,以乙烯和CH2OHCH2CH2COOH为原料制备化合物CH3CH2OOCCH2CH2COOCH2CH3,可以先将CH2OHCH2CH2COOH经过两步氧化得HOOCCH2CH2COOH,乙烯水化得乙醇,乙醇与HOOCCH2CH2COOH发生酯化得CH3CH2OOCCH2CH2COOCH2CH3,
,以乙烯和CH2OHCH2CH2COOH为原料制备化合物CH3CH2OOCCH2CH2COOCH2CH3,可以先将CH2OHCH2CH2COOH经过两步氧化得HOOCCH2CH2COOH,乙烯水化得乙醇,乙醇与HOOCCH2CH2COOH发生酯化得CH3CH2OOCCH2CH2COOCH2CH3,
(1)根据上面的分析可知,化合物C4H6O3中的官能团为羧基和羟基,能与碳酸钠反应的为羧基,故答案为:羧基;
(2)B为CH2=CHCH2COOH,可由C4H7O2Br在NaOH,乙醇溶液,加热条件下发生消去反应生成,故答案为:NaOH,乙醇溶液,加热;CH2=CHCH2COOH;
(3)化合物C4H8O3转化为A的化学方程式为CH2OHCH2CH2COOH $→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:CH2OHCH2CH2COOH $→_{△}^{浓硫酸}$ +H2O;
+H2O;
(4)B为CH2=CHCH2COOH,B的一种同分异构体能发生水解反应,说明有酯基,能发生银镜反应说明有醛基,则符合条件的同分异构体为HCOOCH=CHCH3、HCOOCH2CH=CH2、HCOOC(CH3)=CH2,有3种,
故答案为:3;
(5)以乙烯和CH2OHCH2CH2COOH为原料制备化合物CH3CH2OOCCH2CH2COOCH2CH3,可以先将CH2OHCH2CH2COOH经过两步氧化得HOOCCH2CH2COOH,乙烯水化得乙醇,乙醇与HOOCCH2CH2COOH发生酯化得CH3CH2OOCCH2CH2COOCH2CH3,合成路线为 ,
,
故答案为: .
.
点评 本题考查有机物的推断、官能团、有机反应方程式等,为高考常见题型,侧重于学生的分析能力的考查,注意结合有机物的分子式进行推断,需要学生熟练掌握官能团的性质与转化,题目难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题 | |
| B. | 煤的干馏和石油的分馏均属于化学变化 | |
| C. | 用浸泡过的高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| D. | 福尔马林用于保存海鲜产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| B. | 标准状况下,11.2 L H2O中含有的氢原子数为NA | |
| C. | H2O2分解产生1molO2,转移的电子数为4NA | |
| D. | 1 mol•L-1 CuCl2溶液中含有的氯离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
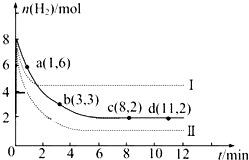 工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:
工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com