
| A.六氟化氙(XeF6) | B.次氯酸(HClO) |
| C.氯化硫(SCl2) | D.三氟化硼(BF3) |


科目:高中化学 来源:不详 题型:单选题
| A.原子半径按X、Y、Z、R、W依次递增 |
| B.Z与Y形成的化合物可作为耐火材料 |
| C.WY2能与强碱反应,但不能与任何酸反应 |
| D.热稳定性:X2R >X2Y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素编号 | 元素结构及性质信息 |
| W | 短周期元素,原子最外层有5个电子,液态单质常用于冷冻生命器官 |
| X | 最外层电子数与内层电子数之差为4,高空中该元素的某种单质具有阻挡紫外线的作用 |
| Y | 最外层电子数与X相同,单质燃烧后产生具有漂白性的气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:CH4>NH3>H2O | B.还原性: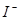 < <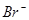 < <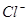 |
| C.酸性:H3PO4>H2SO4>HClO4 | D.原子半径:Na>Mg>O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.中子数为1 | B.质子数为2 |
| C.质量数为3 | D.原子结构示意图是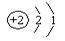 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用乙醇或CCl4可提取碘水中的碘单质 |
| B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同 |
| C.24Mg32S晶体中电子总数与中子总数之比为1∶1 |
| D.H2S和SiF4分子中各原子最外层都满足8电子结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com