
某化学小组在实验室模拟工业生产制备少量氨气,他们设计如下图所示装置(图中夹持装置均已略去)
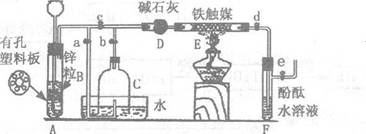
[实验操作]①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗中注入一定量稀硫酸,则A中有氢气生成。打开弹簧夹c、d、e,在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内液面下降到保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是
(2)C瓶内液面下降到保持不变时,A装置内发生的现象是 ,防止了实验装置中压强过大;此时再打开弹簧夹b的主要目的是
(3)在步骤③反应完成后,如何验证反应后的气体中还含有H2、N2?
科目:高中化学 来源: 题型:
| 足量溶液A |
| 充分反应 |
| ||
| 充分反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
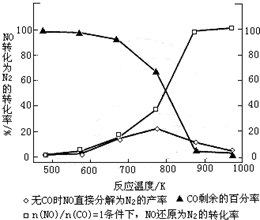
| n(NO) |
| n(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |

| 催化剂 |
| △ |
| 催化剂 |
| △ |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com