
下列说法正确的是( )
A. 化合物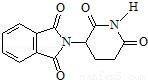 的分子式为C13H9O4N2
的分子式为C13H9O4N2
B. 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH
C. 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
D. 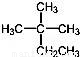 的系统命名为2﹣甲基﹣2﹣乙基丙烷
的系统命名为2﹣甲基﹣2﹣乙基丙烷
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 配制一定物质的量浓度的NaOH溶液,将NaOH固体放在容量瓶中加水至刻度线
B. 由于电流的作用,酸、碱、盐溶于水发生电离
C. 在水溶液中电离出氢离子的化合物属于酸
D. 向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省广州市高一上学期期期末考试化学试卷(解析版) 题型:选择题
同温同压下,等物质的量的SO2和CO2相比较,下列叙述正确的是
① 体积比为 1︰1 ② 密度比为 16︰11
③ 氧原子数比为 1︰1 ④ 质量比为 16︰11
A. ①③④ B. ①②④ C. ②③④ D. 全部
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三2月月考理综化学试卷(解析版) 题型:选择题
下列有关的离子方程式书写正确的是
A. 向铜片中滴加浓硫酸并加热,有刺激性气味气体产生:Cu+4H++SO42-  Cu2++SO2↑+2H2O
Cu2++SO2↑+2H2O
B. 服用阿司匹林过量出现水杨酸(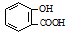 )中毒反应,可静脉注滴NaHCO3溶液:
)中毒反应,可静脉注滴NaHCO3溶液: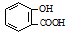 +2HCO3-→
+2HCO3-→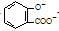 +2CO2↑+2H2O
+2CO2↑+2H2O
C. 20mL1.0mol/L的明矾溶液与10mL3.5mol/L Ba(OH)2溶液混合充分反应:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)2↓
D. 向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三2月月考理科综合化学试卷(解析版) 题型:实验题
天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染.
资料:氰化钠化学式NaCN(C元素+2价,N元素﹣3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢.
I、(1)NaCN水溶液呈碱性,其原因是____________(用离子方程式解释).
(2)双氧水氧化法除NaCN:碱性条件下加入H2O2,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为____________________.
(3)非金属性N______C(填“<”、“>”或“=”),请设计实验证明:_____________。
II、某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放.
[实验一]实验室通过如图装置制备Na2S2O3.

(3)b装置的作用是_______________.
(4)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有__.
(5)实验结束后,在e处最好连接盛__(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1防止拆除装置时污染空气.
[实验二]测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量.
己知:①废水中氰化钠的最高排放标准为0.50mg/L.
②Ag++2CN—=[Ag(CN)2] —,Ag++I—=AgI↓,AgI呈黄色,且CN —优先与Ag+反应.
实验如下.取25.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10﹣4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50mL.
(6)滴定终点的判断方法是_______________.
(7)处理后的废水中氰化钠的含量为_______________mg/L.
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:实验题
实验室以废铁屑为原料制备草酸亚铁晶体(FeC2O4·xH2O)。过程如下:
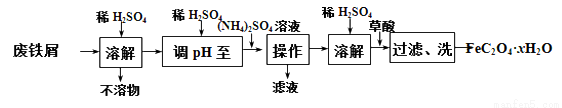
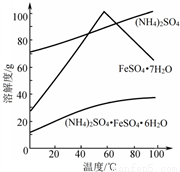
已知:①pH>4时,Fe2+易被氧气氧化;
②相关物质的溶解度曲线如图。
(1)①废铁屑在进行“溶解”前,需要在5%的Na2CO3 溶液中加热数分钟,并洗涤干净,Na2CO3溶液的作用是____________。
②用稀硫酸调溶液pH至1~2的目的:一是抑制Fe2+ 和NH4+的水解;二是 ________。
③操作I是为了得到(NH4)2SO4·FeSO4·6H2O,则操作I应进行蒸发浓缩、结晶、过滤。那么过滤时适宜的温度为__________。
④检验FeC2O4·xH2O沉淀是否洗涤干净的方法是____________。
(2)通常用已知浓度的酸性高锰酸钾溶液测定草酸亚铁晶体的纯度。已知酸性条件下MnO4-转化为Mn2+,写出MnO4-与Fe2+反应的离子方程式:____________。
(3)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备较纯净的FeSO4溶液,再合成FeC2O4·xH2O。请补充完整由硫铁矿烧渣制备纯净FeSO4溶液的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量硫铁矿烧渣中加入足量的稀硫酸充分反应,过滤,____________,过滤,得到较纯净的FeSO4溶液。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
制备5Ca(NO3)2·NH4NO3·10H2O的实验中,过滤出产品后,常温下另取母液(pH<1),向其中加入指定物质,反应后溶液中可大量存在的一组离子是( )
A. 加入过量Na2CO3溶液:Na+、Ca2+、NH4+、NO3-、H+
B. 加入适量NaHCO3溶液:Na+、Ca2+、NH4+、NO3-、HCO3-
C. 加入适量NaOH溶液:Na+、Ca2+、NH4+、NO3-、OH-
D. 加入过量FeSO4和稀硫酸:Fe2+、Fe3+、NH4+、Ca2+、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二下学期第一次模块检测化学试卷(解析版) 题型:选择题
为提纯下列物质(括号内为少量杂质),所选用的除杂式试剂和分离方法正确的是( )
提纯物质 | 除杂试剂 | 分离法 | |
A | KCl溶液(FeCl3) | 氨水 | 过滤 |
B | 乙酸乙酯(乙酸) | 乙醇和浓硫酸 | 分液 |
C | Fe粉(Al粉) | NaOH溶液 | 过滤 |
D | 乙醇(H2O) | 金属钠 | 蒸馏 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江西省协作体高三下学期第一次联考理综化学试卷(解析版) 题型:选择题
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )

A. 在阴极室,发生的电极反应为:2H2O + 2e  2OH -+ H2↑
2OH -+ H2↑
B. 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+ 浓度增大,使平衡2CrO42- + 2H+  Cr2O72- + H2O向右移动
Cr2O72- + H2O向右移动
C. 该制备过程中总反应的化学方程式为4K2CrO4 + 4H2O  2K2Cr2O7 + 4KOH + 2H2↑+ O2↑
2K2Cr2O7 + 4KOH + 2H2↑+ O2↑
D. 测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr) 为d,则此时铬酸钾的转化率为(1-d/2)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com