
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
| X | 中和反应 | 无现象 | 溶解 | 产生氢气 |
| Y | 无现象 | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| Z | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | 无现象 |
| W | 水解反应 | 无现象 | 无现象 | 无现象 |
分析 C3H6O2的有机物有多种同分异构体,现有其中的四种X、Y、Z、W,它们的分子中均含甲基,由实验可知X含-COOH,Y含-OH和-CHO,Z含HCOO-结构,W含-COOC-,以此来解答.
解答 解:C3H6O2的有机物有多种同分异构体,现有其中的四种X、Y、Z、W,它们的分子中均含甲基,由实验可知X含-COOH,Y含-OH和-CHO,Z含HCOO-结构,W含-COOC-,则X为CH3CH2COOH,Y为CH3CHOHCHO,Z为HCOOCH2CH3,Z为CH3COOCH3,
故答案为:CH3CH2COOH;CH3CHOHCHO;HCOOCH2CH3;CH3COOCH3.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与实验能力的考查,注意同分异构体均含甲基,题目难度不大.


科目:高中化学 来源: 题型:解答题
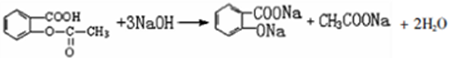 .
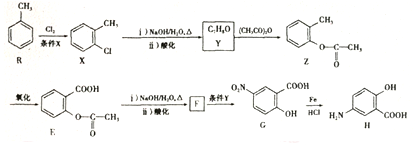
.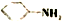 易被氧化;苯环上连有烷基时再引入一个取代基,常取代在烷基的邻、对位,当苯环上连有羧基时则取代在间位.据此以R为原料合成化合物
易被氧化;苯环上连有烷基时再引入一个取代基,常取代在烷基的邻、对位,当苯环上连有羧基时则取代在间位.据此以R为原料合成化合物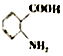 ,参照上述流程设计合成路线:
,参照上述流程设计合成路线: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cl2参加反应转移电子数一定为2NA | |
| B. | 1mol NaHCO3晶体中阳离子数为2NA | |
| C. | 常温常压条件下,14g乙烯和丁烯混合物含有的共用电子对数为3NA | |
| D. | 1ml•L-1 NaCl溶液中含有的Na+数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 第一电离能:③>②>① | B. | 原子半径:③>②>① | ||
| C. | 电负性:③>①>② | D. | 最高化合价:②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LCCl4含有的分子数约为6.02×1023个 | |
| B. | 1L氢气一定比1L氧气质量少 | |
| C. | 含有6.02×1023个Fe3+的Fe2(SO4)3中SO42-的物质的量为3mol | |
| D. | 1molAl3+带有的正电荷数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com