
| c(SO3) |
| c(SO2) |
| n(SO3) |
| n(SO2) |
| c2(SO3) |
| [c2(SO2) ? c(O2)] |


科目:高中化学 来源: 题型:阅读理解
①4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
![]()
③SO3+H2O ![]() H2SO4
H2SO4
其中排放的尾气含少量SO2,为防止污染大气,在排放前应设法进行综合利用。
(1)某硫酸厂每天排放10000m3(换算成标准状况下体积)尾气中含0.2%(体积分数)的SO2,问用NaOH溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4·2H2O)?
(2)如果将一定体积的尾气通入100mL2mol·L-1的NaOH溶液使其完全反应,经测定所得溶液含
(3)工厂在尾气处理制石膏的过程中,中间产物是NaHSO3,调节尾气排放的流量,以取得SO2和NaOH间物质的量的最佳比值,从而提高NaHSO3的产量。现设n(SO2)、n(NaOH)、n(NaHSO3)分别表示SO2、NaOH、NaHSO3的物质的量,且![]() =x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
=x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
x=n(SO2)/n(NaOH) | n(NaHSO3) |
|
|
|
|
|
|
提示:该题取材于接触法制硫酸的过程中对废气SO2的处理,即消除了SO2对空气的污染,又使SO2得到综合利用。该题在能力要求上有一定的深度和坡度。第(1)步考查多步反应的计算,所发生的一系列反应较为复杂,但根据S元素守恒找出关系式,即可得出答案。第(2)步涉及平行反应中混合物的计算。反应方程式为2NaOH+SO2 ![]() Na2SO3+H2O;NaOH+SO2
Na2SO3+H2O;NaOH+SO2 ![]() NaHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。
NaHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
又已知硫酸是一种腐蚀性液体,不便多储存,需随产随销。另外,硫酸的运输价格比较贵,据计算1吨硫酸的运价约为同质量的黄铁矿石的3倍。(注:H2SO4的制取以黄铁矿为原料,流程为:黄铁矿→SO2→SO3→H2SO4)
据以上信息,分析下列条件:
条件Ⅰ:
①A城市郊区有丰富的黄铁矿,水源、能源充足,交通方便。
②A城市需使用硫酸的工业不多,而离它较远的B城市却是一个消耗硫酸甚多的工业城市。
③A城市是一个风光秀丽的旅游城市,对环境保护的要求很高,而且土地价格较贵,土地供应紧张。
条件Ⅱ:
①C城市是重要农业区,需消耗大量的肥料。
②C城市有丰富的磷灰石矿藏,水源、能源充足,土地价格较低,土地供应充足,交通方便。
③磷肥是由磷灰石〔有效成分是Ca3(PO4)2〕与H2SO4作用制得的,制造磷肥需消耗大量的硫酸。
④C城市无磷肥厂和硫酸厂,在相邻的D城市有丰富的黄铁矿资源。
(1)在A、B、C、D四城市中,你认为应该建设硫酸工厂的城市是__________,应该建造磷肥厂的是__________。(填城市的代号)
(2)在建造的硫酸工厂,每天排放1×104 m3(标准状况下)的尾气中含0.2%(体积分数)的SO2。若用NaOH溶液、石灰及氧气处理,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4·2H2O)?
(3)如果将一定体积的尾气通入100 mL 2 mol·L-1 NaOH溶液使其完全反应,经测定所得溶液含16.7 g 溶质。试分析该溶质的成分,通过计算确定溶质成分的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
接触法制H2SO4的基本原理是:
①4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
②2SO2+O2 ![]() 2SO3
2SO3
③SO3+H2O ![]() H2SO4
H2SO4
其中排放的尾气含少量SO2,为防止污染大气,在排放前应设法进行综合利用。
(1)某硫酸厂每天排放10000m3(换算成标准状况下体积)尾气中含0.2%(体积分数)的SO2,问用NaOH溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4·2H2O)?
(2)如果将一定体积的尾气通入100mL2mol·L-1的NaOH溶液使其完全反应,经测定所得溶液含16.7g溶质。试分析溶液的成分,并计算各成分的物质的量。
(3)工厂在尾气处理制石膏的过程中,中间产物是NaHSO3,调节尾气排放的流量,以取得SO2和NaOH间物质的量的最佳比值,从而提高NaHSO3的产量。现设n(SO2)、n(NaOH)、n(NaHSO3)分别表示SO2、NaOH、NaHSO3的物质的量,且![]() =x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
=x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
| x=n(SO2)/n(NaOH) | n(NaHSO3) |
提示:该题取材于接触法制硫酸的过程中对废气SO2的处理,即消除了SO2对空气的污染,又使SO2得到综合利用。该题在能力要求上有一定的深度和坡度。第(1)步考查多步反应的计算,所发生的一系列反应较为复杂,但根据S元素守恒找出关系式,即可得出答案。第(2)步涉及平行反应中混合物的计算。反应方程式为2NaOH+SO2 ![]() Na2SO3+H2O;NaOH+SO2
Na2SO3+H2O;NaOH+SO2 ![]() aHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。
aHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。
查看答案和解析>>
科目:高中化学 来源:2010届靖江高级中学高三第三次模拟考试化学试题 题型:填空题
(10分)近来,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如下: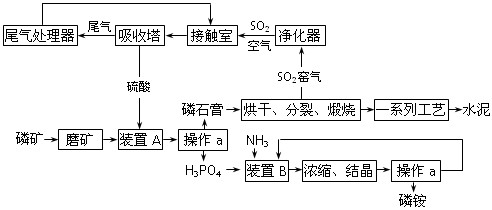
试填空:
⑴ 操作a的名称是 。制硫酸工艺中净化SO2窑气的目的是 。
⑵ 装置B中生成两种酸式盐,它们的化学式分别是 。
⑶ 制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是 (选填字母序号)。
| A.NaOH溶液、酚酞试液 | B.氨水、酚酞试液 |
| C.碘水、淀粉溶液 | D.KMnO4溶液、稀硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com