
| A. | ace | B. | bde | C. | cde | D. | ab |
分析 a.SiO2作为玻璃的成分被消耗,用于刻蚀玻璃,是与氟化氢反应生成四氟化硅;
b.SiO2表现出氧化性,说明硅的化合价降低;
c.SiO2与氢氟酸反应这是二氧化硅的亲氟性的表现;
d.反应④中是符合强酸制弱酸;
e.反应⑤中SiO2中硅与氧的化合价都未变,所以未参加氧化还原反应.
解答 解:a.SiO2作为玻璃的成分被消耗,用于刻蚀玻璃,是与氟化氢反应生成四氟化硅,所以发生反应③,故错误;
b.SiO2表现出氧化性,说明硅的化合价降低,②中硅的化合价降低,故正确;
c.SiO2表现了酸性氧化物的通性,与碱反应生成盐和水,符合通性的是①,而不是③,故错误;
d.反应④中是符合强酸制弱酸,符合用难挥发性的酸酐制取易挥发性酸酐的道理,故正确;
e.反应⑤中SiO2中硅与氧的化合价都未变,所以未参加氧化还原反应,故正确;
故选:B.
点评 本题实际考查物质间的反应规律,熟记物质间的反应规律及反应条件才能很好的解答本题.


科目:高中化学 来源: 题型:选择题
| A. | 可以用浓溴水区分苯和甲苯 | |
| B. | 淀粉和纤维素水解的最终产物均为果糖 | |
| C. | 实验室中,可以用电石和饱和食盐水制取乙炔 | |
| D. | H2N-CH2-COOH和 缩合只能形成一种二肽 缩合只能形成一种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,它是重要的化工原料,它在一定条件下可发生以下变化:
,它是重要的化工原料,它在一定条件下可发生以下变化:
 或
或 .
. +n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$
+n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下将0.1mol•L-1NH4Cl溶液与0.05mol•L-1NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 常温下物质的量浓度相等的①NH4HSO4②CH3COONH4③NH4Cl三种溶液中c(NH4+):①>③>② | |
| C. | 0.1mol•L-1的NaHA溶液,其pH=11,则溶液中:c(HA-)>c(OH-)>c(A2-)>c(H2A) | |
| D. | 在相同条件下,将足联AgCl加入等体积的①0.01mol•L-1 KCl②0.1mol•L-1 KCl溶液③蒸馏水三种液体中,所能溶解的AgCl质量关系为:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
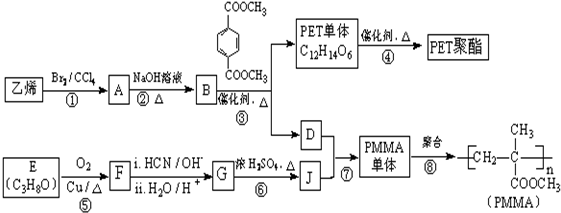
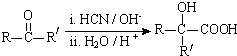 (R、R′代表烃基,可相同也可不同)
(R、R′代表烃基,可相同也可不同)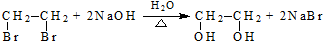 .
. .
.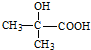 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com