
【题目】一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)Z(g),经60s达到平衡,生成0.3mol Z,下列正确的是( )
A.60s内以X浓度变化表示的反应速率为0.001 mol/(L?s)
B.将容器体积变为20L,Z的平衡浓度变为原来的 ![]()
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的正反应为吸热反应
【答案】A
【解析】解:A.达到平衡时Z的平均反应速率为:v(Z)= ![]() =0.0005mol/(Ls),反应速率与化学计量数成正比,则60s内以X浓度变化表示的反应速率为:v(X)=2v(Z)=0.001 mol/(Ls),故A正确; B.将容器容积变为20L时,物质的压强减小,平衡向体积增大的方向移动,即逆向移动,Z的物质的量减小,即小于0.3mol,Z的新平衡浓度将小于原平衡浓度的
=0.0005mol/(Ls),反应速率与化学计量数成正比,则60s内以X浓度变化表示的反应速率为:v(X)=2v(Z)=0.001 mol/(Ls),故A正确; B.将容器容积变为20L时,物质的压强减小,平衡向体积增大的方向移动,即逆向移动,Z的物质的量减小,即小于0.3mol,Z的新平衡浓度将小于原平衡浓度的 ![]() ,故B错误;
,故B错误;
C.增大压强后,平衡向着正反应方向移动,则Y的转化率增大,故C错误;
D.若升高温度,X的体积分数增大,说明逆反应为吸热反应,则正反应为放热反应,故D错误;
故选A.
【考点精析】利用化学平衡的计算对题目进行判断即可得到答案,需要熟知反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,将3molA和1molB投入容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是 ( )
xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是 ( )
A. x=2
B. 2min时,B的浓度为0.4mol/L
C. 0~2min内B的反应速率为0.2mol·L-·min-
D. 此时A的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
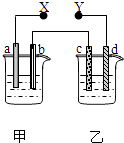
【题目】如图X、Y分别是直流电源的两极,通电后发现a极板质量增加,d极板有无色无臭的气体放出,符合这一情况的是( )
选项 | a 极板 | d极板 | X极板 | 乙中溶液 |
A | 锌 | 铜 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中所发生的化学变化,属于加成反应的是
A.光照射甲烷和氯气的混合气体
B.在镍做催化剂的条件下,苯与氢气反应
C.乙醇在铜或银做催化剂的条件下与氧气反应
D.乙酸在浓硫酸做催化剂的条件下与乙醇反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在恒容密闭容器中,进行反应:A(s)+2B(g)![]() 2C(g) ΔH<0。下列说法正确的是
2C(g) ΔH<0。下列说法正确的是
A. 达到平衡后,从容器中移走部分反应物A,则正反应速率将下降
B. 当混合气体的密度不再发生变化时,说明反应达到平衡状态
C. 改变反应前A与B的投料比,ΔH将发生相应的改变
D. 向反应体系中继续通入足量B气体,A有可能反应完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是一种常见的化肥,某工厂用石膏、NH3、H2O、CO2制备(NH4)2SO4的工艺流程如下:
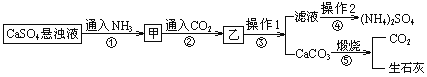
下列说法正确的是
A. 通入NH3和CO2的顺序可以颠倒
B. 操作1为过滤,操作2为蒸馏
C. 步骤②中反应的离子方程式为CaSO4+2NH3+CO2+H2O=CaCO3↓+2NH4++SO42-
D. 通入的NH3和CO2均应过量,且工艺流程中CO2可循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. ![]() 由3种单体加聚得到
由3种单体加聚得到
B. 氨基酸溶于过量氢氧化钠溶液中生成的离子,在电场作用下向阴极移动
C. 甲苯与足量H2加成产物的一氯取代物有5种
D. 分子式为C4H6O2并能与饱和NaHCO3溶液反应生成CO2的有机物有3种(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐( 主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
![]()
(1)请写出镓(与铝同主族的第四周期元素)的原子结构示意图_________。
(2)为尽量少引入杂质,试剂①应选用______(填标号)。理由是______________。
A.HCl溶液 B.H2SO4 溶液 C.氨水 D.NaOH溶液
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是________(用离子方程式表示)。
(4)科学研究证明NaAlO2 在水溶液中实际上是Na[Al(OH)4](四羟基合铝酸钠),易拉罐溶解过程中主要反应的化学方程式为___________________。
(5)常温下,等pH的NaAlO2 和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=__________。
(6)已知室温下,Kw=10×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com