
【题目】镁及其化合物有着广泛用途。工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下:
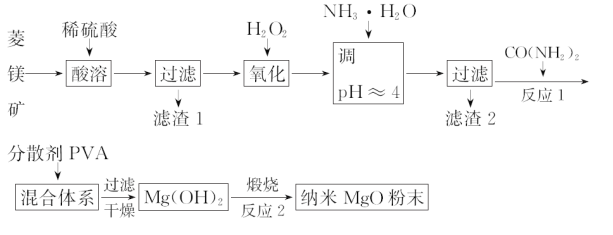
(1)滤渣1为______________________。
(2)加入H2O2氧化时,发生反应的离子方程式为______________________。
(3)在实验室煅烧滤渣2制得的金属氧化物为____________(填化学式),需要的仪器除酒精灯、三脚架、泥三角以外,还需要______________(填名称)。
(4)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,该反应中反应物的质量之比为________。
(5)25℃时,加入CO(NH2)2至开始产生沉淀,当Mg2+全部沉淀时溶液的c(OH-)=__________(已知25℃,Ksp[Mg(OH)2]=1.96×10-11)。
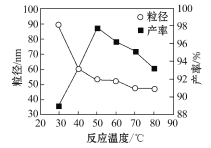
(6)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制备 纳米MgO。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明是纳米MgO存在的简单方法是____________。如图为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为____________。
【答案】(1)SiO2;(2)2Fe2++H2O2+2H+=2Fe3++2H2O;(3)Fe2O3,坩埚;
(4)10∶9(或9∶10);(5)1.4×10-3mol·L-1;
(6)用一束光照射,在侧面会看到一条光亮的通路(或答丁达尔现象);50℃。
【解析】
试题分析:(1)根据菱镁矿的成分,MgCO3和FeCO3和稀硫酸反应,SiO2是酸性氧化物,不与稀硫酸反应,因此滤渣1是SiO2;(2)加入过氧化氢的目的,是把Fe2+氧化成Fe3+,离子反应方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;(3)调节pH=4,使Fe3+全部以Fe(OH)3形式沉降出来,因此煅烧Fe(OH)3,得到产物是Fe2O3,煅烧时用到仪器是坩埚;(4)反应方程式为CO(NH2)2+3H2O=CO2+2NH3·H2O,反应物的质量比=60:54=10:9;(5)根据Ksp=c(Mg2+)×c2(OH-),代入数值,c(Mg2+)=1×10-5mol·L-1,c(OH-)=1.4×10-3mol·L-1;(6)纳米分散系属于胶体,验证胶体常用丁达尔效应;根据图,最佳温度是50℃,产率最高,因此选择50℃。


科目:高中化学 来源: 题型:
【题目】食盐是一种常用的食品添加剂。新鲜鱼、肉用食盐腌渍后可以延长保存期,是因为( )
A.NACl中的Cl-有杀菌作用 B.浓食盐水中含O2少,细菌无法生存
C.由于渗透作用使细菌失水死亡 D.由于渗透作用使鱼、肉细胞失水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应A(s) +3B(g)![]() 2C(g)+D(g)已达平衡状态的是(其中只有B气体有颜色)
2C(g)+D(g)已达平衡状态的是(其中只有B气体有颜色)
A.混合气体的压强
B.混合气体的密度
C.气体的平均分子量
D.气体的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评价 |
A | Fe3O4与稀硝酸反应: 2Fe3O4+18H+===6Fe3++H2↑+8H2O | 正确 |
B | 向碳酸镁中加入稀盐酸: CO | 错误,碳酸镁不应写成离子形式 |
C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO | 正确 |
D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1∶2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池产生电流的本质原因是( )
A.原电池中溶液能电离出自由移动的离子
B.有两根导线将两个活泼性不同的电极连接
C.电极上进行的氧化还原反应的生成物为电子
D.电极上进行的氧化还原反应中发生了电子的转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的说法中正确的是( )
A. 钠在空气中燃烧只生成白色的氧化钠固体
B. 燃着的镁条伸入盛满二氧化碳的集气瓶中不能继续燃烧
C. 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作
D. 铁能与硫酸发生反应,故不能用铁制容器贮存浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温常压下,1mol CH4的体积是22.4L
B. 1molFe在氯气中完全燃烧失去电子数为2NA
C. 用激光笔照射可鉴别Fe(OH)3胶体和FeCl3溶液
D. 用焰色反应可鉴别NaCl和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时X和盐酸和缓地进行反应.其中反应速率最大的是( )
A.20mL 3mol/L 的X溶液
B.20mL 2mol/L 的X溶液
C.10mL 4mol/L的X溶液
D.10mL 2mol/L的X溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com