
| A、两种难溶电解质,其中Ksp小的溶解度一定小 |
| B、溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀 |
| C、所谓沉淀完全就是用沉淀剂将溶液中的某一离子除净 |
| D、相同温度下,AgCl固体在0.01 mol?L-1 KI溶液中的溶解的质量比在0.01mol?L-1 KNO3溶液中大,但Ksp不变 |


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
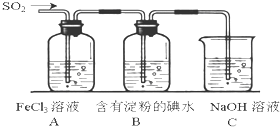 某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:
某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过渡 |
| ② | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| ③ | CO2 | SO2 | 通过盛KMnO4(H+)溶液烧洗气瓶,再通过浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 溶解、过滤、蒸发结晶 |
| A、①②④ | B、③④ |
| C、②③④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol |
| B、2.4mol |
| C、0.075mol |
| D、0.05mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
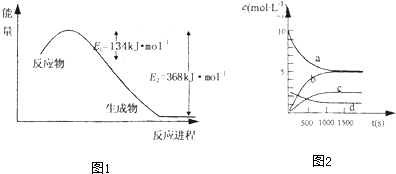 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少N的氧化物在大气中的排放是环境保护的重要内容之一.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少N的氧化物在大气中的排放是环境保护的重要内容之一.| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )| A、上述反应△H<0 |
| B、上述反应△H>0 |
| C、a>b |
| D、a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔融状态下该晶体能导电 |
| B、K3C60中碳元素显-3价 |
| C、K3C60中只有离子键 |
| D、C60与12C互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com