
【题目】将5.60 g铁投入100 mL某浓度的盐酸中,铁和盐酸恰好完全反应。
求:(1)5.60 g铁的物质的量
(2)所用盐酸中HCl中的物质的量浓度
(3)反应中生成的H2在标准状况下的体积
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 做衣服的棉和麻均与淀粉互为同分异构体
B. 制饭盒、高压锅等的不锈钢是合金
C. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某块光卤石(KCl·MgCl2·6H2O)中含5.3250 Cl-,则该光卤石的物质的量为_________mol
(2)0.15molH2SO4的质量是___________g,能和___________mol NaOH完全反应,该硫酸所含氢元素的质量与__________mol H2PO4或标准状况下__________L HCl中所含氢元素的质量相同。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-离子,则ACl2的摩尔质量是_________;ACl2的化学式是____________。
(4) 0.3 mol的氧气和0.22 mol的臭氧(O3),它们的质量______________,它们所含的分子数__________,原子数__________,(以上三空填“相等”或“不相等”)它们的体积比(同温、同压)是__________。
(5)己知在标况下的四种气体①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S ④0.2molNH3用相应的序号填写下列空白
体积最大的是__________;质量最小的是__________;含氢原子数最多的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.标准状况下,11.2L苯中含有C﹣H键的数目为3NA
B.常温下,1.0LpH=13的Ba(OH)2溶液中含有的OH﹣数目为0.1NA
C.常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子
D.电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案:

回答下列问题:
(1)试剂1是 ,作用是 ;
(2)试剂2是 ,作用是 ,发生的离子反应为: ;如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的 ,若不能,其原因是 。
(3)如何检验第①步实验已基本完成 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一支25mL滴定管,内盛溶液液面在15.00mL刻度处,当将滴定管内液体全部排出时,所得液体的体积是
A. 10.00mL B. 15.00mL C. 小于10.00mL D. 大于10.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,体积均为1 L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。
容器 | 甲 | 乙 | 丙 | 丁 |
起始投料量 | 2 mol SO2+1 mol O2 | 1 mol SO2+0.5 mol O2 | 2 mol SO3 | 2 mol SO2+2 mol O2 |
反应放出或吸收的热量(kJ) | a | b | c | d |
平衡时c(SO3) (mol·L-1) | e | f | g | h |
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 制普通玻璃的主要原料是烧碱、石灰石、石英
B. SiO2是光导纤维的主要成分,晶体硅可用于制作半导体材料
C. 实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液
D. 盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯、铁的某些化合物在工业生产和生活中有着重要的作用。
(1)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。主要有两种制备方法:
方法一:
工业上常常用 KClO3和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 ,生成5molClO2转移电子 mol。
方法二:
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
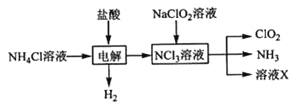
NCl3溶液和NaClO2溶液发生反应的离子方程式 。
X中大量存在的阴离子有_____ 。
(2)铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
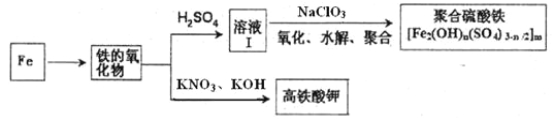
①检验固体铁的氧化物中铁的化合价,应使用的试剂是 (填标号)。
A.稀硫酸 B.稀硝酸 C.KSCN溶液 D.酸性高锰酸钾溶液
②在溶液Ⅰ中加入NaClO3写出其氧化Fe2+的离子方程式: 。
③Fe2O3与KNO3和KOH的混合物加热共融可制得高铁酸鉀。完成并配平化学方程式:
□Fe2O3+□KNO3+□KOH——□ +□KNO2+□ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com