
| A. | CH2═CH2+HCl $→_{△}^{催化剂}$CH3CH2Cl | |
| B. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| C. | 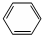 +Br2 $\stackrel{FeBr_{3}}{→}$ +Br2 $\stackrel{FeBr_{3}}{→}$ 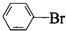 +HBr +HBr | |
| D. | CH3CH2 Br+NaOH $→_{△}^{乙醇}$ CH2=CH2↑+Na Br+H2O |
分析 A.碳碳双键转化为单键;
B.甲烷中H被Cl取代;
C.苯环上H被Br取代;
D.-Br转化为碳碳双键.
解答 解:A.CH2═CH2+HCl $→_{△}^{催化剂}$CH3CH2Cl为乙烯的加成反应,故A选;
B.CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl为取代反应,故B不选;
C. +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$  +HBr为取代反应,故C不选;
+HBr为取代反应,故C不选;
D.CH3CH2 Br+NaOH $→_{△}^{乙醇}$ CH2=CH2↑+NaBr+H2O为卤代烃的消去反应,故D不选;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应类型的判断,题目难度不大.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H++2e-═H2↑ | B. | Fe-2e-═Fe2+ | ||
| C. | 4OH--4e-═2H2O+O2↑ | D. | Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6$\stackrel{酒化酶}{→}$2C2H6O+2CO2↑ | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | HC≡CH+HCl$\stackrel{一定条件}{→}$CH2=CHCl | D. | 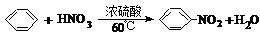 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
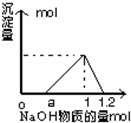 往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )
往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )| A. | 1:3 | B. | 1:4 | C. | 1:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人类历史上使用最早的合金是青铜 | |
| B. | 金属钛有可能在21世纪得到广泛运用 | |
| C. | 广泛运用铝合金,是因为铝不能与酸、碱、O2等反应 | |
| D. | 目前世界上用途最广的合金是钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com