
”¾ĢāÄæ”æŹµŃéŹŅÓĆĆܶČĪŖ1.25gmL©1”¢ÖŹĮæ·ÖŹżĪŖ36.5%µÄÅØŃĪĖįÅäÖĘ240mL 0.1molL©1µÄŃĪĖį£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÅØŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ
£Ø2£©ÅäÖĘ 240mL 0.1molL©1 µÄŃĪĖį
Ó¦ĮæČ”ÅØŃĪĖįĢå»ż/mL | ӦєÓĆČŻĮæĘæµÄ¹ęøń/mL |
£Ø3£©ÅäÖĘŹ±£¬ĘäÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ£Ø×ÖÄø±ķŹ¾£¬Ćæøö×ÖÄøÖ»ÄÜÓĆŅ»“Ī £© £®
A£®ÓĆ30mLĖ®Ļ“µÓÉÕ±ÄŚ±ŚŗĶ²£Į§°ō23“Ī£¬Ļ“µÓŅŗ¾ł×¢ČėČŻĮæĘ棬Õńµ“
B£®ÓĆĮæĶ²»“Č·ĮæČ”ĖłŠčµÄÅØŃĪĖįµÄĢå»ż£¬µ¹ČėÉÕ±ÖŠ£¬ŌŁ¼ÓČėÉŁĮæĖ®£ØŌ¼30mL£©£¬ÓĆ²£Į§°ōĀżĀż½Į¶Æ£¬Ź¹Ęä»ģŗĻ¾łŌČ
C£®½«ŅŃĄäČ“µÄŃĪĖįŃŲ²£Į§°ō×¢ČėČŻĮæĘæÖŠ
D£®½«ČŻĮæĘæøĒ½ō£¬Õńµ“£¬Ņ”ŌČ
E£®øÄÓĆ½ŗĶ·µĪ¹Ü¼ÓĖ®£¬Ź¹ČÜŅŗ°¼ŅŗĆęĒ”ŗĆÓėæĢ¶ČĻßĻąĒŠ
F£®¼ĢŠųĶłČŻĮæĘæÄŚŠ”ŠÄ¼ÓĖ®£¬Ö±µ½ŅŗĆę½Ó½üæĢ¶ČĻß12cm“¦
£Ø4£©ČōŹµŃéÖŠÓöµ½ĻĀĮŠĒéæö£¬¶ŌŃĪĖįČÜŅŗµÄĪļÖŹµÄĮæÅضČÓŠŗĪÓ°Ļģ£ØĢī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°²»±ä”±£©£æ
¢ŁÓĆÓŚĻ”ŹĶŃĪĖįµÄÉÕ±Ī“Ļ“µÓ£¬ £®
¢ŚČŻĮæĘæÖŠŌÓŠÉŁĮæÕōĮóĖ®£¬ £®
¢Ū¶ØČŻŹ±¹Ū²ģŅŗĆęø©ŹÓ£¬ £®
£Ø5£©ČōŹµŃé¹ż³ĢÖŠ³öĻÖČēĻĀĒéæöČēŗĪ“¦Ąķ£æ
¢Ł¶ØČŻŹ±¼ÓÕōĮóĖ®Ź±³¬¹żĮĖæĢ¶Č £®
¢ŚĻņČŻĮæĘæÖŠ×ŖŅĘČÜŅŗŹ±ÓŠ¹öŅŗ²»É÷ÓŠČÜŅŗ½¦³ö £®
¢Ū¶ØČŻŅ”ņŗó·¢ĻÖŅŗĆęĻĀ½µ
”¾“š°ø”æ
£Ø1£©12.5mol£®l©1
£Ø2£©2.0£»250
£Ø3£©B”¢C”¢A”¢F”¢E”¢D
£Ø4£©Ę«µĶ£»²»±ä£»Ę«øß
£Ø5£©ÖŲŠĀÅäÖĆ£»ÖŲŠĀÅäÖĆ£»ĪŽŠčŌŁÅä
”¾½āĪö”æ½ā£ŗ£Ø1£©ÅØŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ ![]() =12.5mol/L£¬
=12.5mol/L£¬
ĖłŅŌ“š°øŹĒ£ŗ12.5mol£®l©1£»
£Ø2£©ÅäÖĘ240mL0.1molL©1µÄŃĪĖį£¬Ó¦Ń”Ōń250mLČŻĮæĘ棬Źµ¼ŹÅäÖĘ250mLČÜŅŗ£¬ÉčŠčŅŖÅØŃĪĖįĢå»żĪŖV£¬ŌņŅĄ¾ŻČÜŅŗĻ”ŹĶ¹ż³Ģ ÖŠČÜÖŹµÄĪļÖŹµÄĮæ²»±äµĆ£ŗV”Į12.5mol/L=0.1mol/L”Į250mL£¬½āµĆV=2.0mL£»
ĖłŅŌ“š°øŹĒ£ŗ2.0£»250£»
£Ø3£©ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ²½Öč£ŗ¼ĘĖć”¢³ĘĮ攢Čܽā”¢×ŖŅĘ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČµČ£¬¹ŹÕżČ·µÄĖ³ŠņĪŖ£ŗBCAFED£»
ĖłŅŌ“š°øŹĒ£ŗBCAFED£»
£Ø4£©¢ŁÓĆŅŌĻ”ŹĶÅØĮņĖįµÄÉÕ±Ī“Ļ“µÓ£¬µ¼ÖĀČÜÖŹĘ«ÉŁ£¬ÅضČĘ«µĶ£»
ĖłŅŌ“š°øŹĒ£ŗĘ«µĶ£»
¢ŚČŻĮæĘæÖŠŌÓŠÉŁĮæÕōĮóĖ®£¬¶ŌČÜŅŗµÄÅضČĪŽÓ°Ļģ£¬ČÜŅŗµÄÅØ¶Č²»±ä£»
ĖłŅŌ“š°øŹĒ£ŗ²»±ä£»
¢Ū¶ØČŻŹ±¹Ū²ģŅŗĆęø©ŹÓ£¬µ¼ÖĀČÜŅŗµÄĢå»żĘ«Š”£¬ČÜŅŗµÄÅضČĘ«øߣ»
ĖłŅŌ“š°øŹĒ£ŗĘ«øߣ»
£Ø5£©¢Ł¶ØČŻŹ±¼ÓÕōĮóĖ®Ź±³¬¹żĮĖæĢ¶Č£¬ČÜŅŗµÄÅضČĘ«Š”£¬ŠčŅŖÖŲŠĀÅäÖĆ£»ĖłŅŌ“š°øŹĒ£ŗÖŲŠĀÅäÖĆ£»
¢ŚĻņČŻĮæĘæÖŠ×ŖŅĘČÜŅŗŹ±ÓŠ¹öŅŗ²»É÷ÓŠČÜŅŗ½¦³ö£¬ČÜŅŗµÄÅضČĘ«Š”£¬ŠčŅŖÖŲŠĀÅäÖĆ£»ĖłŅŌ“š°øŹĒ£ŗÖŲŠĀÅäÖĆ£»
¢Ū¶ØČŻŅ”ņŗó·¢ĻÖŅŗĆęĻĀ½µ£¬ČÜŅŗµÄÅØ¶Č²»±ä£»ĖłŅŌ“š°øŹĒ£ŗĪŽŠčŌŁÅ䣮
”¾æ¼µć¾«Īö”æĶعżĮé»īŌĖÓĆÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ£¬ÕĘĪÕÅäÖĘĪļÖŹµÄĮæÅضČČÜŅŗŹ±£¬ĻČÓĆÉÕ±¼ÓÕōĮóĖ®ÖĮČŻĮæĘææĢ¶ČĻß1cm”«2cmŗó£¬ŌŁøÄÓĆ½»Ķ¶µĪ¹Ü¼ÓĖ®ÖĮæĢ¶ČĻß¼“æÉŅŌ½ā“š“ĖĢā£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĪļÖŹµÄĖµ·ØÕżČ·µÄŹĒ
A.²£Į§”¢ĢÕ“É”¢Ė®Äą”¢¹āµ¼ĻĖĪ¬µÄ»Æѧ×é³É¶¼ŹĒ¹čĖįŃĪ
B.Ņŗ°±Ęū»ÆŹ±ŅŖĪüŹÕ“óĮæµÄČČ£¬æÉÓĆ×÷ÖĘĄä¼Į
C.¶žŃõ»Æ¹č²»ÓėĒæĖį·“Ó¦£¬æÉÓĆŹÆÓ¢Ę÷ĆóŹ¢·ÅĒā·śĖį
D.ÉśŹÆ»ŅÄÜÓėĖ®·“Ó¦£¬æÉÓĆĄ“øÉŌļĀČĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§Ķź³ÉČēĻĀĢ½¾æŹµŃé£ŗ
ŹµŃéÄæµÄ£ŗ±Č½ĻCl2”¢Br2”¢I2ČżÖÖµ„ÖŹµÄŃõ»ÆŠŌĒæČõ
ŹµŃéŅ©Ę·£ŗNaBrČÜŅŗ”¢KIČÜŅŗ”¢ĀČĖ®”¢µķ·ŪČÜŅŗ
ŹµŃé¼ĒĀ¼£ŗ
ŹµŃé²½Öč | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ČÜŅŗ±äĪŖ»ĘÉ« | Ńõ»ÆŠŌ£ŗCl2£¾Br2 |
| ČÜŅŗ±äĪŖ»ĘÉ« | Ńõ»ÆŠŌ£ŗ |
| ČÜŅŗµÄŃÕÉ«ÓÉ»ĘÉ«±äĪŖĄ¶É« |
·“Ė¼ÓėĘĄ¼Ū£ŗ
£Ø1£©²½Öč¢Ł·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ £®
£Ø2£©¼ģŃé¢ŚÖŠĖłµĆ»ĘÉ«ČÜŅŗŗ¬I2µÄĮķŅ»ÖÖ·½·ØŹĒ£Ø¼ņŹöŹµŃé²Ł×÷ŗĶĻąÓ¦µÄŹµŃéĻÖĻó£©
£®
£Ø3£©ÄćČĻĪŖÉĻŹöŹµŃéÉč¼Ę£ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©“ļµ½ŹµŃéÄæµÄ£¬ĄķÓÉŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ĻĀĮŠĪļÖŹæÉŅŌÓĆĀĮÖĘČŻĘ÷Ź¢×°µÄŹĒ£Ø £©
A.ĒāŃõ»ÆÄĘČÜŅŗ
B.Ļ”ĮņĖį
C.ÅØŃĪĖį
D.ÅØĻõĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŹµŃéŹŅŗĻ³ÉĮĖŅ»ÖÖæÉČܵĽšŹōĀČ»ÆĪļ£ØRClx£©£¬ĪŖĮĖ²ā¶ØøĆ½šŹōĀČ»ÆĪļµÄ³É·Ö£¬ŃŠ¾æČĖŌ±×öĮĖŅŌĻĀŹµŃé£ŗČ”ĪļÖŹµÄĮæÅضČĪŖ0.05molL©1µÄ½šŹōĀČ»ÆĪļ£ØRClx£© ČÜŅŗ20mL£¬Ź¹Ö®Ē”ŗĆÓė20mL 0.15molL©1µÄAgNO3ČÜŅŗĶźČ«·“Ó¦£®ŌņøĆĀČ»ÆĪļµÄ»ÆѧŹ½ĪŖ£Ø £©
A.RCl
B.RCl2
C.RCl3
D.RCl4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ×°ÖĆÓĆÓŚŹµŃéŹŅÖʱø°±Ęų²¢×öÅēČŖŹµŃ飬²»ÄÜ“ļµ½ŹµŃéÄæµÄŹĒ£Ø £©
A. ¼ģ²éĘųĆÜŠŌ
¼ģ²éĘųĆÜŠŌ
B. Öʱø°±Ęų
Öʱø°±Ęų
C. ĪüŹÕ°±Ī²Ęų
ĪüŹÕ°±Ī²Ęų
D. ÅēČŖŹµŃé
ÅēČŖŹµŃé
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×é»ÆŗĻĪļÖŠ£¬»Æѧ¼üĄąŠĶĶźČ«ĻąĶ¬µÄŹĒ£Ø £©
A. HClŗĶNaOH B. Na2OŗĶNa2O2
C. CO2ŗĶCS2 D. Ca(OH)2,ŗĶNa2S
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµČĢå»ż£¬ÅØ¶Č¾łĪŖ0.lmol/LµÄČżÖÖČÜŅŗ£ŗ¢ŁCH3 COOHČÜŅŗ”¢¢ŚHSCNČÜŅŗ”¢¢ŪNaHCO3ČÜŅŗ£¬¼ŗÖŖ½«¢Ł”¢¢Ś·Ö±šÓė¢Ū»ģŗĻ£¬ŹµŃé²āµĆ²śÉśµÄCO2ĘųĢåĢå»ż£Øv£© Ėꏱ¼ä£Øt£©±ä»ÆµÄŹ¾ŅāĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
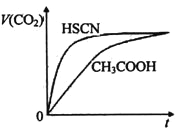
A. ĪļÖŹĖįŠŌµÄ±Č½ĻCH3COOH>HSCN>H2CO3
B. ·“Ó¦½įŹųŗóĖłµĆĮ½ČÜŅŗÖŠ£¬c (CH3COC- ) >c (SCN-)
C. ÉĻŹöČżÖÖČÜŅŗÖŠÓÉĖ®µēĄėµÄc (OH-)“󊔣ŗ NaHCO3>CH3COOH>HSCN
D. CH3COOHČÜŅŗŗĶNaHCO3ČÜŅŗ·“Ó¦ĖłµĆČÜŅŗÖŠ£ŗc (CH3COO-) +c (CH3COOH) =0.10mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬·“Ó¦C(s)+H2O(g)![]() CO(g)+H2(g)ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠĢõ¼žµÄøıä¶ŌĘä·“Ó¦
CO(g)+H2(g)ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠĢõ¼žµÄøıä¶ŌĘä·“Ó¦
ĖŁĀŹ¼øŗõĪŽÓ°ĻģµÄŹĒ
A. Ōö¼ÓCOµÄĮæ
B. ½«ČŻĘ÷µÄĢå»żĖõŠ”Ņ»°ė
C. ±£³ÖĢå»ż²»±ä£¬³äČėN2Ź¹ĢåĻµŃ¹ĒæŌö“ó
D. ±£³ÖŃ¹Ēæ²»±ä£¬³äČėN2Ź¹ČŻĘ÷Ģå»ż±ä“ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com