
(每空2分共计12分)某可逆反应从0—2分钟进行过程中, 在不同反应时间各物质的量的变化情况如 图所示。
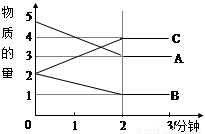
①则该反应的的反应物是 ,生成物是 ,
②化学方程式为 ;
③反应开始至2分钟时,能否用C表示反应速率?
④若能,其反应速率为 ,若不能,则其原因为 ;
⑤2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____ 状态。
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:2013届辽宁省沈阳铁路实验中学高三第一次月考化学试卷(带解析) 题型:填空题
(每空3分共计10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。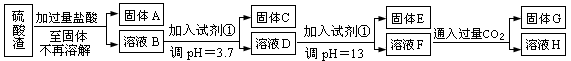
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省高三第一次月考化学试卷(解析版) 题型:填空题
(每空3分共计10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。
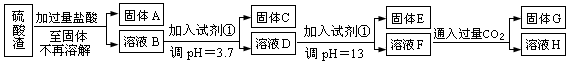
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是 ;(任写一点)
(4)H中溶质的化学式: ;
(5)计算溶液F中c(Mg2+)= (25℃时,氢氧化镁的Ksp=5.6×10-12)
查看答案和解析>>
科目:高中化学 来源: 题型:
(每空2分共计12分)某可逆反应从0—2分钟进行过程中, 在不同反应时间各物质的量的变化情况如 图所示。
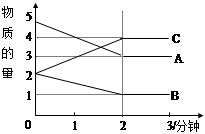
①则该反应的的反应物是 ,生成物是 ,
②化学方程式为 ;
③反应开始至2分钟时,能否用C表示反应速率?
④若能,其反应速率为 ,若不能,则其原因为 ;
⑤2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____ 状态。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com