
| A. | 乙醇分子的比例模型: | |
| B. | 蔗糖、麦穿糖、淀粉、纤维素充全水解都只生成葡萄糖 | |
| C. | 《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 | |
| D. | 许多国家十分重视海水资源的综合利用,从海水中可获得的物质有氧、溴、碘、钠、镁、铝、烧碱、氢气、食盐、淡水 |
分析 A、比例模型表示原子的比例大小关系、原子之间的连接顺序与空间结构,不能表示原子之间的成键情况;
B、蔗糖水解后生成的葡萄糖和果糖;
C、碳酸钙俗称石灰石,高温能分解;
D、海洋含有丰富的资源,海水是资源的宝库.
解答 解:A、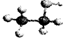 表明乙醇分子中成键情况,是乙醇的球棍模型,而不是比例模型,故A错误;
表明乙醇分子中成键情况,是乙醇的球棍模型,而不是比例模型,故A错误;
B、蔗糖、麦穿糖、淀粉、纤维素均能水解,蔗糖水解后生成的葡萄糖和果糖,不只是葡萄糖,故B错误;
C、碳酸钙俗称石灰石,高温煅烧能分解为CaO和二氧化碳,故石灰指的是碳酸钙,故C错误;
D、海洋含有丰富的资源,海水是资源的宝库,从海水中可以提取镁、溴、碘、钠、铝的单质以及氯化钠等,通过电解饱和食盐水还能氢气、氯气和氢氧化钠,电解水能获得氢气和氧气,通过海水的蒸馏可以获得淡水等,故D正确.
故选D.
点评 本题考查了有机物的球棍模型和比例模型的区别以及糖类和水解产物和海水资源的综合利用等,考查范围比较广,但难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )| X | Y | Z | |
| A | 强电解质 | 电解质 | 化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 碱性氧化物 | 金属氧化物 | 氧化物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素.X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体.请回答下列问题(用元素符号或化学式表示):
已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素.X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体.请回答下列问题(用元素符号或化学式表示): ,其第一电离能反常地低于同周期前一种元素,原因是Mg原子的3s2全充满,反而比Al原子3p1稳定.
,其第一电离能反常地低于同周期前一种元素,原因是Mg原子的3s2全充满,反而比Al原子3p1稳定. ,该分子的空间构型是直线型.
,该分子的空间构型是直线型.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列说法中正确的是( )
下列说法中正确的是( )| A. | 异丙烯苯与苯互为同系物 | |
| B. | 异丙烯苯不能发生取代反应 | |
| C. | 异丙苯的一溴代物有5种 | |
| D. | 0.5mol 异丙苯完全燃烧消耗氧气5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物:CO2、SiO2、SO2、NO2 | |
| B. | 碱:烧碱、纯碱、苛性钾、氢氧化钡 | |
| C. | 混合物:盐酸、漂白粉、水煤气、氢氧化铁胶体 | |
| D. | 碱性氧化物:Na2O、CaO、MgO、Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| B. | 碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32-═CaCO3↓+2OH- | |
| C. | NaHCO3溶液中滴加NaOH溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 往FeI2溶液中通入过量氯气:Cl2+2Fe2+═2Cl-+2Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胃酸过多的病人都可以服用氢氧化钠、氢氧化铝、碳酸钠等中和胃酸的药 | |
| B. | 使用青霉素时,不用进行皮试可直接静脉注射 | |
| C. | 阿司匹林是一种治感冒药,具有解热镇痛作用 | |
| D. | 麻黄碱有止咳平喘的作用,运动员比赛前若身体不适可服用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com