
【题目】下列说法正确的是( )
A. 电离能大的元素,不易失电子,易得到电子,表现非金属性
B. 电离能大的元素其电负性必然也大
C. 电负性最大的非金属元素形成的含氧酸的酸性最强
D. 电离能最小的元素形成的氧化物的水化物的碱性最强
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为: ![]() ,下列关于该电池工作时的说法正确的是
,下列关于该电池工作时的说法正确的是![]()
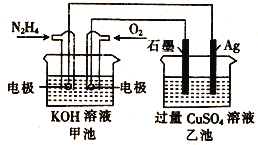
A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为![]()
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗![]()
![]() 时,乙池中理论上最多产生
时,乙池中理论上最多产生![]() 固体
固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,同时几乎不影响生成的氢气总量,不可以采取的措施是( )
A.加热,升高溶液温度
B.加入适量的水
C.加入少量CuSO4溶液
D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆![]() 甲醇燃料电池的工作原理如图所示.
甲醇燃料电池的工作原理如图所示.
![]() 该电池工作时,b口通入的物质为______,c口通入的物质为______.
该电池工作时,b口通入的物质为______,c口通入的物质为______.
![]() 该电池负极的电极反应式为:______.
该电池负极的电极反应式为:______.
![]() 工作一段时间后,当
工作一段时间后,当![]() 甲醇完全反应生成
甲醇完全反应生成![]() 时,有______
时,有______![]() 个电子转移.
个电子转移.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2SO2(g)+O2(g)![]() 2SO3(g)达到平衡。下列说法正确的是
2SO3(g)达到平衡。下列说法正确的是
容器 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | SO2或SO3平衡转化率 | ||
c(SO2) | c(O2) | c(SO3) | c(SO3) | |||
I | 723 | 0.2 | 0.1 | 0 | 0.16 | a1 |
II | 723 | 0.4 | 0.2 | 0 | a2 | |
III | 823 | 0 | 0 | 0.2 | a3 | |
A. 达到平衡时,a1+a3>1
B. 达到平衡时,容器中的压强: PII>PI>PIII
C. 达到平衡时,容器III中的逆反应速率比容器I中的大
D. 若起始时,向容器I中充入0.16molSO2、0.04molO2和0.16molSO3,则此时反应向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用高锰酸钾分解制氧气的反应,测定室温下的气体摩尔体积,实验装置如下。

部分实验步骤:
①装好实验装置。
② 。
③把适量的高锰酸钾粉末放入干燥的试管中,准确称量试管和高锰酸钾粉末的质量为m g。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热。
⑥测量收集到的气体体积。
⑦准确称量试管和残留物的质量为n g。
⑧测量实验室的温度。
回答下列问题。
(1)实验步骤的第②步是 ________________________________________________。
(2)测量收集到的气体体积,应注意的事项有:
①_____________________________________________________________________;
②_____________________________________________________________________;
③视线与凹液面最低处相平。
(3)如果实验中得到的氧气体积是p L,水蒸气的影响忽略不计,则室温下气体摩尔体积的计算式为__________(含m、n、p)。
(4)假定其他操作均正确,未恢复至室温就读数会导致实验结果___________________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是

A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com