
向一定浓度的下列物质的澄清溶液中通入过量的CO2气体,最后肯定没有沉淀生成的是( )
①Ca(OH)2②Na2CO3③CaCl2④Ca(ClO)2⑤Na2SiO3.
A.①③④
B.②③④
C.①②③⑤
D.①②③④
考点:钠的重要化合物;氯、溴、碘及其化合物的综合应用;硅和二氧化硅.
分析:向Ca(OH)2、Ca(ClO)2溶液分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成;饱和Na2CO3溶液中通入CO2,会析出NaHCO3晶体;CO2与CaCl2不反应,Na2SiO3溶液中通入CO2,会析出硅酸沉淀,据此进行判断.
解答: 解:①Ca(OH)2溶液中分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成,故①正确;
②Na2CO3,饱和Na2CO3溶液中通入CO2,会析出NaHCO3晶体,故②错误;
③CaCl2,CO2与CaCl2不反应,故③正确;
④Ca(ClO)2溶液分别通入过量CO2,最终生成Ca(HCO3)2,没有沉淀生成,故④正确;
⑤Na2SiO3溶液分别通入过量CO2,最终生成硅酸沉淀,有沉淀生成,故⑤错误;
故选A.
点评:本题考查了离子反应发生条件、元素及其化合物的性质等,题目难度不大,注重了基础知识的考查,应该熟练掌握离子反应发生的条件.


科目:高中化学 来源: 题型:
关于原子轨道的说法正确的是( )
|
| A. | 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
|
| B. | CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
|
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 |
|
| D. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化方式成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 卤代烃在NaOH存在下水解生成的有机物都是醇 |
|
| B. | 所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
|
| C. |
|
|
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用图所示装置来制取乙酸乙酯,回答下列问题:
(1)请写出本实验中发生的主要反应方程式 .
(2)配置混合溶液时,加入试剂的正确顺序是 (填“A”或“B”).
A.先加乙醇,再慢慢注入浓硫酸和乙酸 B.先加浓硫酸,再慢慢注入乙醇和乙酸
(3)浓硫酸的作用是 .
(4)饱和Na2CO3溶液的作用是 .
(5)实验完成后,右边试管液面上有透明的不溶于水的油状液体生成.若要分离10mL该液体混合物需要用到的主要玻璃仪器是 ,这种分离方法叫做 .
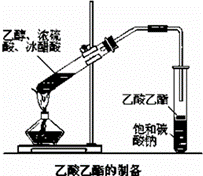
查看答案和解析>>
科目:高中化学 来源: 题型:
泡沫灭火机内装的药液之一是NaHCO3饱和溶液,而不选用更廉价的Na2CO3饱和溶液,其原因是( )
①质量相同的两种钠盐,NaHCO3与足量酸反应产生的CO2比Na2CO3多
②产生相同体积 (同温,同压)的CO2,消耗酸的量NaHCO3比Na2CO3少
(同温,同压)的CO2,消耗酸的量NaHCO3比Na2CO3少
③NaHCO3与酸反应比Na2CO3快得多
④NaHCO3比Na2CO3稳定,便于长期保存.
A.只有①③
B.只有②③
C.①②③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe粉,充分反应后产生的NO气体在标准状况下的体积为( )
A.36 L
B.28 L
C.22.4 L
D.11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法中正确的是 ( )
A.在该反应中维生素C作催化剂
B.砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷可能是+3价砷
C.因为河虾中含有砷元素,所以不能食用 D.上述反应中维生素C作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.在反应CaH2+2H2O===Ca(OH)2+2H2↑中,水作氧化剂
B.根据反应Cu+H2SO4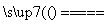 CuSO4+H2↑可推出Cu的还原性比H2的强
CuSO4+H2↑可推出Cu的还原性比H2的强
C.反应3NO2+H2O===2HNO3+NO中氧化剂和还原剂的物质的量之比是3∶1
D.因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3===2NaIO3+Cl2不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2C | 试管内壁都有水珠 | 两种物质均受热分解 |
| B | 向稀的苯酚水溶液中滴加饱 和溴水 | 生成白色沉淀 | 产物三溴苯酚溶于水 |
| C | 向含I-的无色溶液中滴加少量铁盐溶液,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Fe3+ |
| D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com