
分析 溶液中溶质物质的量相同时,与碱反应后溶液呈中性,硫酸是二元酸,醋酸是弱酸;醋酸与氢氧化钠溶液反应生成醋酸钠,反应后为中性,则c(OH-)=c(H+),结合电荷守恒判断溶液中离子浓度大小.
解答 解:体积和浓度相同a:CH3COOH、b:HCl、c:H2SO4三溶液,假设溶质为1mol,分别与同浓度的烧碱溶液反应,要使反应后溶液的pH为7,CH3COOH是弱酸,恰好中和生成醋酸钠溶液呈碱性,所以中性时需要烧碱小于1mol;氯化氢和1mol氢氧化钠恰好反应溶液呈中性;1molH2SO4和2mol恰好反应需要氢氧化钠2mol,所需烧碱溶液的体积由大到小关系为:c>b>a;
所得溶液为中性,则c(OH-)=c(H+),根据溶液中的核电荷数可知:c(CH3COO-)=c(Na+),溶液中离子浓度大小为:c(CH3COO-)=c(Na+)>c(OH-)=c(H+),
故答案为:c>b>a;c(CH3COO-)=c(Na+)>c(OH-)=c(H+).
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的灵活应用能力.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:选择题
| A. | SO3溶于水后能导电,故SO3为电解质 | |
| B. | 在蒸馏水中滴加浓H2SO4,KW不变 | |
| C. | CaCO3难溶于稀硫酸,也难溶于醋酸 | |
| D. | KCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液与过量的浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向Ca(ClO)2溶液通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| C. | FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4 Fe3++2H2O | |
| D. | CuSO4溶液与少量的Ba(OH)2溶液:Ba2+十SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
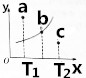 某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:
某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:| 密闭容器 | A | B | C |
| n(起始状态)/mol | 4 | 2 | 0 |
| n(平衡状态)/mol | 2.8 | 1.4 | 1.2 |
| 密闭容器 | 甲 | 乙 | 丙 | 丁 | |
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(A)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(B)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| A的平衡转化率 | 80 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| B. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 固体悬浮微粒是造成雾霾天气的一种重要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
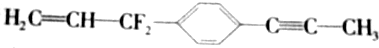 为已知结构,下列叙述中正确的是( )
为已知结构,下列叙述中正确的是( )| A. | 除苯环外的其余碳原子有可能都在同一条直线上 | |
| B. | 在同一平面上的原子最多有19个 | |
| C. | 12个碳原子不可能都在同一个平面上 | |
| D. | 12个碳原子有可能都在同一个平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D元素处于元素周期表中第二周期VIA族 | |
| B. | 四种元素的原子半径:A<B<C<D | |
| C. | B、D的最高价氧化物具有相似的物理性质和化学性质 | |
| D. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
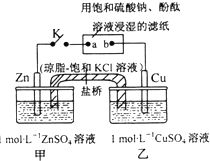
| A. | Zn极上发生还原反应 | |
| B. | 电子沿Zn→a→b→Cu路径流动 | |
| C. | 片刻后,乙池中c(Cu2+)减小,c(SO42-)基本不变,溶液不再保持电中性 | |
| D. | 片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com