
FeCl3溶液和Fe(OH)3胶体共同具备的性质是
A.加入饱和NaCl溶液都产生沉淀 B.加入盐酸先产生沉淀,后沉淀溶解
C.分散质的粒子都能通过滤纸 D.都能产生丁达尔效应
科目:高中化学 来源:2016-2017学年青海省高二上月考一化学卷(解析版) 题型:选择题
生产液晶显示器的过程中使用的化学清洗剂NF3是 一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 | N≡N | F—F | N—F |
键能:kJ/mol | 941.7 | 154.8 | 283.0 |
下列说法中正确的是( )
A.过程N2(g) 2N(g)放出能量
2N(g)放出能量
B.过程N(g)+3F(g) NF3(g)放出能量
NF3(g)放出能量
C.反应N2(g)+3F2(g) 2NF3(g)的ΔH>0
2NF3(g)的ΔH>0
D.NF3吸收能量后如果没有化学键的断裂与生成,仍能可能发生化学反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上半期考试化学卷(解析版) 题型:选择题
在一密闭容器中进行反应:2SO2(g)+ O2(g)
O2(g) 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol ·L-1、0.1 mol ·L-1、0.2 mol ·L-1。当反应达平衡时,可能存在的数据是
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol ·L-1、0.1 mol ·L-1、0.2 mol ·L-1。当反应达平衡时,可能存在的数据是
A.SO2为0.4 mol ·L-1,O2为0.2 mol ·L-1 B.SO2为0.25 mol ·L-1
C.SO2、SO3均为0.15 mol ·L-1 D.SO3为0.4 mol ·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:实验题
现有含淀粉、NaCl、Na2SO4、CaCl2的混合溶液,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
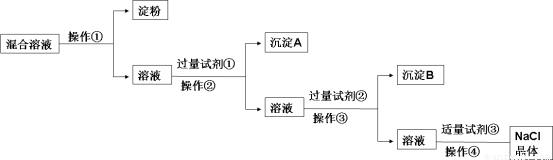
(1)操作①是利用胶体不能通过 而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:
试剂①___________________;试剂③_____________________。
(3)判断试剂①已过量的操作是:__________________。
(4)控制试剂③适量的方法是:__________________。
(5)试剂②的作用(用化学方程式表示):__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气(F2),于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是
A.1∶2 B.1∶3 C.1∶4 D.1∶6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学卷(解析版) 题型:选择题
食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
品名 | 蔬菜苏打饼 |
配料 | 面粉、鲜鸡蛋 、精炼食用植物油、白砂糖 、奶油、食盐、脱水青菜、橙汁 |
保质期 | 十二个月 |
生产日期 | 2016 年8月20日 |
对上表中各种配料的成分的理解正确的是
A.富含蛋白质的是鸡蛋 B.富含维生素的是脱水青菜和橙汁
C.富含糖类的物质只有白砂糖 D.富含油脂的是精炼食用植物油和奶油
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学卷(解析版) 题型:选择题
关于食物的酸碱性,下列说法正确的是
A.食物溶于水后的溶液中pH小于7,则为成酸性食物
B.由碳、氮、硫、磷等元素组成的富含蛋白质的食物,习惯称为成酸性食物
C.蔬菜、水果多含钾、钠、钙、镁等盐类,习惯称为酸性食物
D.口感呈酸性的食物不一定是酸性食物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学卷(解析版) 题型:选择题
下表对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 缺乏维生素A | 引发贫血症 | Ⅰ对,Ⅱ对,无 |
B | 人体缺铁 | 引发骨质疏松 | Ⅰ对,Ⅱ错,有 |
C | 人体缺钙 | 引发甲状腺肿大 | Ⅰ对,Ⅱ对,有 |
D | 缺乏维生素C | 引发坏血病 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上半期考试化学试卷(解析版) 题型:填空题
【物质结构与性质】硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为 。
(2)锗、砷、硒的第一电离能大小排序为 。H2SeO4的酸性比H2SeO3的强,其原因是 。
(3)H2SeO3的中心原子杂化类型是 ;SeO32-的立体构型是 。与SeO42-互为等电体的分子有(写一种物质的化学式即可) 。
(4)H2Se属于 (填:极性或非极性)分子;单质硒的熔点为217℃,它属于 晶体。
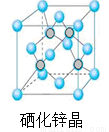
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为 ;若该晶胞密度为ρg•cm-3,硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为___________pm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com