
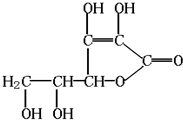
分析 (1)由结构可知分子式;
(2)滴加紫色石蕊试液,试液变红,具有酸的性质;
(3)维生素C由于能防治坏血病,为抗坏血酸;
(4)服用维生素C可解除中毒,这说明维生素C将铁离子转化为亚铁离子;高锰酸钾具有强氧化性.
解答 解:(1)由结构可知分子式为C6H8O6,故答案为:C6H8O6;
(2)滴加紫色石蕊试液,试液变红,具有酸的性质,故答案为:酸;
(3)维生素C由于能防治坏血病,又称为抗坏血酸,故答案为:抗坏血酸;
(4)服用维生素C可解除中毒,这说明维生素C将铁离子转化为亚铁离子,则具有还原性;高锰酸钾具有强氧化性,与维生素C发生氧化还原反应,高锰酸钾褪色,
故答案为:还原;酸性KMnO4溶液褪色.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系及信息为解答的关键,侧重分享与应用能力的考查,题目难度不大.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量时,将胆矾晶体直接放在托盘天平的右盘上 | |
| B. | 准确称取16.0g胆矾,溶于水,待溶液恢复到室温,转移至1000mL容量瓶中,定容 | |
| C. | 准确称取25.0g胆矾,溶于水,待溶液恢复到室温,转移至1000mL容量瓶中,定容 | |
| D. | 定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用醋、石灰水验证蛋壳中含有碳酸盐 | |
| B. | 用碘酒检验汽油中是否含有不饱和烃 | |
| C. | 用鸡蛋清、食盐、水完成蛋白质的溶解、盐析实验 | |
| D. | 用米汤检验食用加碘盐(含KIO3)中含有碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=△H1+△H2 | B. | △H3=△H1+2△H2 | C. | △H3=2△H2-△H1 | D. | △H3=△H1-△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和SiO2 | B. | CCl4和KCl | C. | NaOH和CaCl2 | D. | CO2和H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com