
 烃A是一种重要的化工原料.己知A在标准状况下的密度为1.16g•L-1,B可发生银镜反应.它们之间的转化关系如图:请回答:
烃A是一种重要的化工原料.己知A在标准状况下的密度为1.16g•L-1,B可发生银镜反应.它们之间的转化关系如图:请回答:分析 A在标准状况下的密度为1.16g•L-1,则A的摩尔质量为1.16g/L×22.4L/mol=26g/mol,B可发生银镜反应,则B为醛,由流程图可知,A加水反应生成B,B氧化生成D,B加氢还原生成C,C与D发生反应生成乙酸乙酯,则A为CH≡CH,B为CH3CHO,C为CH3CH2OH,D为CH3COOH,以此来解答.
解答 解:(1)由上述分析可知,A为CH≡CH,官能团名称为碳碳叁键,故答案为:碳碳叁键;
(2)由上述分析可知,B为CH3CHO,反应④的原子利用率达100%,则CH3CHO发生加成反应生成CH3COOCH2CH3,该反应的化学方程式是2CH3CHO$\stackrel{一定条件}{→}$CH3COOCH2CH3,故答案为:2CH3CHO$\stackrel{一定条件}{→}$CH3COOCH2CH3;
(3)A.C为CH3CH2OH与乙酸发生酯化反应生成乙酸乙酯和水,为可逆反应,则在一定条件下合成乙酸乙酯不能实现原子利用率100%,故A错误;
B.反应②为还原反应,③为氧化反应、⑤为酯化反应,所以类型各不相同,故B正确;
C.乙酸乙酯与水不相溶,可以用分液漏斗分离乙酸乙酿和水的混合物,故C错误;
D.乙酸乙酯在氢氧化钠溶液中水解生成乙酸钠和乙醇,不可逆,较在稀硫酸中更完全,故D正确;
故答案为:BD.
点评 本题考查有机物的推断,为高频考点,把握信息及官能团的变化为解答的关键,侧重分析与推断能力的考查,注意A为乙炔,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H+、Ca2+、NO3-、CO32- | B. | K+、Na+、Cl-、SO42- | ||
| C. | Ag+、Na+、Cl-、K+ | D. | NH4+、K+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漏斗、烧杯、蒸发皿、酒精灯 | B. | 量筒、烧杯、试管夹、蒸发皿 | ||
| C. | 玻璃棒、蒸发皿、漏斗、集气瓶 | D. | 铁架台、天平、长颈漏斗、酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳 | B. | 钠 | C. | 硫 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将1 mol HCl溶于1 L水中得到的溶液 | |
| B. | 将1 mol SO3溶于1 L水中得到的溶液 | |
| C. | 将1 mol H2SO4溶于水制成的体积1 L的溶液 | |
| D. | 将0.5 mol SO3溶于水制成的体积1 L的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 中的※C原子为手性碳原子;若一个碳原子上连着2个C=C(如
中的※C原子为手性碳原子;若一个碳原子上连着2个C=C(如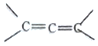 )时,极不稳定,不存在.现有某链烃C7H10的众多同分异构体中:
)时,极不稳定,不存在.现有某链烃C7H10的众多同分异构体中: ═CH-CH3
═CH-CH3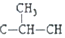 ═CH2
═CH2 -CH≡CH3
-CH≡CH3 ;
; .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸溶液中和氢氧化钠溶液 | B. | 硫酸溶液中和氢氧化钡溶液 | ||
| C. | 盐酸溶解氧化铜 | D. | 盐酸溶解氢氧化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某溶液中加入BaCl2溶液,再加入盐酸 | 证明溶液中是否含SO42- |
| B | 加热铝箔,熔化的铝不滴落 | 铝表面的氧化膜熔点高,包在熔化的铝外面 |
| C | Cl2能使湿润的紫色石蕊试纸先变红后褪色 | Cl2具有漂白性 |
| D | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色 | 验证亚硫酸的不稳定性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com