
科目:高中化学 来源:不详 题型:单选题
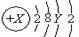 。则X、Y及该原子3p能级上的电子数分别为( )
。则X、Y及该原子3p能级上的电子数分别为( )| A.18、6、4 | B.20、8、6 | C.18、8、6 | D.15~20、3~8、1~6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ;B ; H ;F
;B ; H ;F 
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
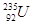 是重要的工业原料,铀浓缩一直为国际社会关注。下列有关
是重要的工业原料,铀浓缩一直为国际社会关注。下列有关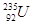 的说法正确的是
的说法正确的是A.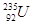 原子核中含有92个中子 原子核中含有92个中子 | B.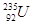 原子核外有143个电子 原子核外有143个电子 |
C.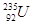 与 与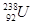 互为同位素 互为同位素 | D.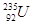 与 与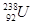 是两种不同的元素 是两种不同的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
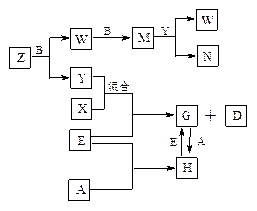
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 原子个数比为1:1的共价化合物,请写出其分子式: ;
原子个数比为1:1的共价化合物,请写出其分子式: ;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com