
科目:高中化学 来源: 题型:阅读理解
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||


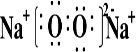
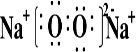

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
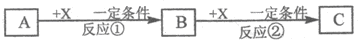
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是( )
A.H2 B.HCHO C.C12H22O11 D.维生素C
(2)Vc极不稳定,具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2====C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下:取10 mL 6 mol·L-1 CH3COOH,加入100 mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.20 g样品,溶解于上述冷却的溶液中。加入1 mL淀粉指示剂,立即用浓度为0.05 mol·L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00 mL I2溶液。
①为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
②计算样品中维生素C的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
2009年8月,陕西省凤翔县长青镇马道口村和邻村孙家南头村的村民们自发到宝鸡各大医院检测发现,两村数百名婴幼儿及儿童绝大多数被检测出体内铅含量超标,其中部分超标严重,已达到中毒标准。两村民居南北环抱着的一家年产铅锌20万吨的冶炼企业,被疑与此有关。
⑴铅(原子序数为82)位于元素周期表的 周期 族,已知+2价铅比+4价铅稳定,+4价铅有较强的氧化性。将PbO2与浓盐酸加热反应产生黄绿色的气体,写出该反应的离子方程式 ,将SO2通入棕色PbO2的悬浊液中会产生白色沉淀,写出该反应的化学方程式 。
⑵铅锭冶炼厂采用火法冶炼铅,铅在自然界中以方铅矿(PbS)的形式存在,主要生产过程是先煅烧方铅矿制成PbO,再用CO还原PbO制备铅。上述生产过程中的主要化学方程式为 、 。
⑶铅蓄电池是典型的可充电型电池,它的正负极板是惰性材料,电池总反应式为:![]() 。放电时正极的电极反应式是 ;
。放电时正极的电极反应式是 ;
电解液中H2SO4的浓度将(填“变大”“变小”或“不变“);当外电路通过电子2mol时,理论上负极板的质量增加 g。
⑷铅在工业中应用广泛,如为了增强彩釉的亮度,陶瓷业在釉中常加入少量的铅。铅在酸性溶液中容易溶解,生成+2价铅进入人体,写出铅“吃醋”的化学方程式: 。汽车工业为提高发动机的使用寿命,常在汽油中加入抗震剂四乙基铅的分子式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com