
科目:高中化学 来源: 题型:
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因是( )
A.电子由激发态向基态跃迁时以光的形式释放能量
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.在电流的作用下,氖原子与构成灯管的物质发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铝及其化合物的叙述正确的是( )
A.铝罐可久盛食醋(2014·福建理综,6C)
B.氢氧化铝可作胃酸的中和剂(2014·四川理综,1D)
C.明矾用作净水剂不涉及化学变化(2014·重庆理综,1A)
D.铝与Fe2O3发生铝热反应,反应后固体物质增重(2014·新课标全国卷Ⅱ,9C)
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种化合物均含有某种短周期常见元素,它们的转化关系如图所示,其中A的溶液为澄清溶液,C为难溶于水的白色固体,E则易溶于水,取A的溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
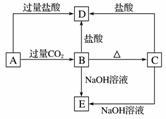
(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B:________________________________________________________________________;
A→D:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是____________。
①MgSO4溶液 ②NaCl溶液 ③Na2SO4溶液 ④饱和澄清石灰水 ⑤Ca(HCO3)2溶液 ⑥CuSO4溶液 ⑦饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28 g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
| A | 1 mol | 2NA | |
| B | 22.4 L | 1 mol | |
| C | 106 g | 1 mol | |
| D | 106 g | 2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
有关NaHCO3和Na2CO3的性质,以下叙述错误的是( )
A.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C.等质量NaHCO3和Na2CO3与盐酸完全反应,前者消耗盐酸较多
D.等物质的量的NaHCO3和Na2CO3与足量盐酸反应产生CO2一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.NA表示阿伏加德罗常数,1 mol Na被完全氧化生成Na2O2,失去2NA个电子(2013·广东理综,9D)
B.Na2O2用作呼吸面具的供氧剂涉及氧化还原反应(2012·广东理综,10A)
C.苏打是面包发酵粉的主要成分之一(2014·福建理综,6D改编)
D.NaHCO3的热稳定性大于Na2CO3(2012·重庆理综,7B)
查看答案和解析>>
科目:高中化学 来源: 题型:
脱硫技术能有效控制SO2对空气的污染。
(1)向煤中加入石灰石可减少燃烧产物中SO2的含量,该反应的化学方程式是____________________________ 。
(2)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO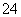 、Br-、HCO
、Br-、HCO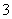 等。含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
等。含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
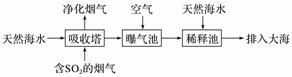
①向曝气池中通入空气的目的是_______________________________________________。
②通入空气后,曝气池中的海水与天然海水相比,浓度有明显不同的离子是________(填字母)。
a.Cl- b.SO c.Br- d.HCO
c.Br- d.HCO
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可得到NaOH,同时得到H2SO4,其原理如图所示。(电极材料为石墨)
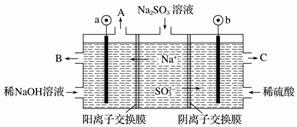
①图中a极连接电源的______(填“正”或“负”)极,C口流出的物质是________。
②SO 放电的电极反应为________________________。
放电的电极反应为________________________。
③电解过程中阴极区碱性明显增强,用平衡移动的原理解释碱性增强的原因:________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com