
| A. | v(NH3)=0.25 mol•L-1•min-1 | B. | v(O2)=0.35mol•L-1•min-1 | ||
| C. | v(NO)=0.01 mol•L-1•s-1 | D. | v(H2O)=0.3 mol•L-1•min-1 |
分析 化学反应速率与化学计量数之比越大,则反应速率越快,以此来解答.
解答 解:化学反应速率与化学计量数之比越大,则反应速率越快,
A.$\frac{0.25}{4}$=0.0625;
B.$\frac{0.35}{5}$=0.07;
C.v(NO)=0.01 mol•L-1•s-1=0.6 mol•L-1•min-1,$\frac{0.6}{4}$=0.15;
D.$\frac{0.3}{6}$=0.05,
所以反应速率大小顺序是C>B>A>C,则反应速率最快的是C,故选C.
点评 本题考查化学反应速率快慢比较,明确同一可逆反应中各物质反应速率与计量数关系即可解答,易错选项是C,注意比较反应速率单位要统一,为易错题.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
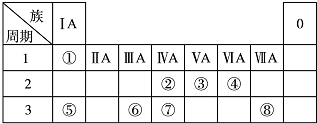
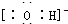 .
.| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| 1 | ||
| 2 |
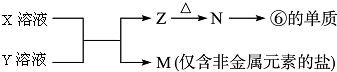
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A3BC4 | B. | A2(BC4)3 | C. | A2BC3 | D. | A2BC4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO-、H+、Na+、K+ | B. | NH4+、OH-、Ba2+、Cl- | ||
| C. | Ca2+、NO3-、Ba2+、K+ | D. | NO3-、Ba2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴水混合,振荡静置,溴水层褪色 | |
| B. | 乙烯通入酸性髙锰酸钾溶液中,溶液褪色 | |
| C. | 乙烯通入溴的四氛化碳溶液中,溶液褪色 | |
| D. | 甲烷与氯气混合光照,气体颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
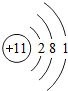 ;
;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com