
【题目】下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硝酸
D.SO2和Na2SO3溶液都能使氯水褪色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中完全正确的一组是( )
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池中,若Cu极生成0. 2 g H2,则电路通过电子0.2NA
③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
④常温常压下,16 g O3所含的原子数为NA
⑤1 mol C10H22分子中共价键总数为31NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦标准状况下22. 4 L水中含分子数为NA
A. ①②③④⑤ B. ②④⑤⑥⑦ C. ②④⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇来源丰富、价格低廉,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是:CO(g)+2H2(g) ![]() CH3OH(g) △H = —91kJ/mol。
CH3OH(g) △H = —91kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = —580kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = —570kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H = ________________。
若在恒温恒容的容器内进行反应CO(g)+2H2(g) ![]() CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
A.CO百分含量保持不变 B.容器中混合气体的密度不变化
C.有1个H—H键生成的同时有 3个C—H键生成 D.容器中混合气体的压强不变化
(2)制甲醇所需要的H2,可用下列反应制取:H2O(g)+CO(g) ![]() H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
①该温度下,反应进行一阶段时间后,测得H2的浓度为0.5mol/L-1,则此时该反应v(正)__________v(逆)(填“>”、“<”或“=”);
②若反应温度不变,达到平衡后,H2O的转化率为________。
(3)某实验小组设计了甲醇以氢氧化钾为电解质溶液的燃料电池装置。
①试想该电池工作时,OH— 向_______极移动(填“负”或“正”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为______________________。总反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当前材料科学的发展方兴未艾。B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_________;Ti原子核外共有____种运动状态不同的电子。
(2)BF3分子与NH3分子的空间结构分别为____、______;NH3分子是_____分子(填“极性”或“非极性”);BF3与NH3反应生成的BF3·NH3分子中含有的化学键类型有______,在BF3·NH3中B原子的杂化方式为____________。
(3)N和P同主族。科学家目前合成了N4分子,该分子中N—N键的健角为_______。
(4)晶格能:NaN3____KN3(选填“>”、“<”或“=”)
(5)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子,在[Cu(NH3)4]2+中提供孤电子对的成键原子是______。不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为________。己知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸(H2C=CHCOOH)与乙醇(CH3CH2OH)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃。
回答下列问题:
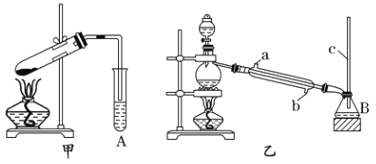
(1)仪器M的名称为_________,仪器A、B中的溶液均为 _________。
(2)甲、乙两套装置中效果比较好的装置是_______,原因是__________。
(3)乙装置中冷凝水应该从______(填“a”或“b”)口进入。
(4)若7.2g丙烯酸与5.2g乙醇完全反应,则理论上生成的丙烯酸乙酯的质量为________。(精确到小数点后一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,
2NH3(g) ΔH<0,
(1)在恒温恒压条件下进行,反应正向进行的是________;反应逆向进行的是________;处于平衡状态的是________;无法判断是否达到平衡的是________。
A.单位时间内生成1mol N2,同时生成3mol NH3
B.单位时间内生成3mol N2,同时生成6mol N—H键
C.混合气体的密度不再随时间而改变
D.容器中气体的压强不再随时间而改变
(2)在一定温度下某恒容密闭容器中,充入3molH2和1mol的N2,2min达到平衡状态时,总的气体的物质的量变为原来的9/10,则此时N2的转化率为__________;
若此时放出的热量为18.44 kJ,则其热化学方程式为______________________________ .
根据所求出的热化学方程式,且已知1mol氮氮三键断裂需要为945.8kJ的能量,1mol氢氢键断裂需要436 kJ的能量,求1molN-H键断裂吸收的能量_____。
(3)氨气可用作碱性燃料电池的燃料,电池反应为4NH3+3O2═2N2+6H2O,
则氨燃料电池的负极电极反应为________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 足量乙酸与碳酸钠溶液反应: 2 CH3COOH +CO32-→ 2CH3COO-+CO2↑+H2O
B. 醋酸溶液与新制氢氧化铜反应: 2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液中通入少量二氧化碳: 2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2 A![]() B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
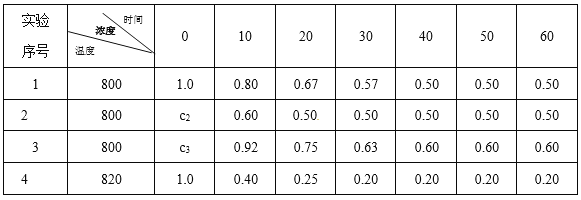
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20 min时间内A的平均反应速率为___________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1。
(3)设实验3的反应速率为v3。,实验1的反应速率为v1,则v3_____vl(填“>”、“="或“<”)。
(4)比较实验4和实验1,可推测该反应是_______(填“吸热”或“放热”)反应。
理由是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352 g,置于铂舟并放入燃烧管中,不断通入氧气流。用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144 g和0.528 g,生成物完全被吸收。试回答以下问题:
(1)维生素C中碳的质量分数是_____________,氢的质量分数____________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com