
请仔细观察下列五种装置的构造示意图,完成下列问题:
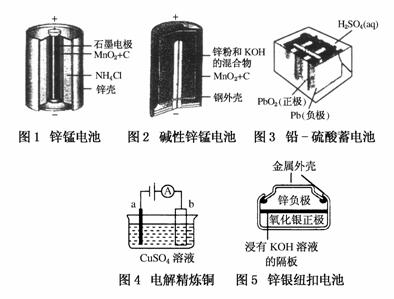
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2,则负极的电极反 应式______________________。
应式______________________。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是______________________________。
(3)铅-硫酸蓄电池放电过程中,H2SO4浓度______(填“变大”“变小”或“不变”),充电时阴极的电极反应式为____________________________。
(4)电解精炼铜时,a极是________(填“纯铜”或“粗铜”)。锌银纽扣电池在工作过程中________(填物质名称)被还原。
解析 (1)原电池的负极发生氧化反应,根据元素化合价变化知锌失电子,负极的电极反应为Zn+2OH--2e-===Zn(OH)2。(2)碱性锌锰电池用锌粉替代了原锌锰电池的锌壳,增大了反应物的接触面积,加快了反应速率,故放电电流大。(3)铅蓄电池在放电过程中消耗硫酸,所以硫酸浓度变小,充电时阴极PbSO4得电子生成Pb,发生反应PbSO4+2e-===Pb+SO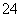 。(4)电解精炼铜时,粗铜作阳极,纯铜作阴极,则a极为纯铜。锌银纽扣电池中锌作负极,氧化银作正极,正极发生还原反应,即氧化银被还原。
。(4)电解精炼铜时,粗铜作阳极,纯铜作阴极,则a极为纯铜。锌银纽扣电池中锌作负极,氧化银作正极,正极发生还原反应,即氧化银被还原。
答案 ( 1)Zn+2OH--2e-===Zn(OH)2
1)Zn+2OH--2e-===Zn(OH)2
(2)碱性锌锰电池用锌粉替代了原锌锰电池的锌壳,增大了反应物的接触面积,加快了反应速率,故放电电流大 (3)变小 PbSO4+2e-===Pb+SO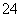
(4)纯铜 氧化银


科目:高中化学 来源: 题型:
下列说法中,正确的是 ( )
A.SO2水溶液能导电,所以SO2是电解质
B.Na2CO3既是钠盐又是碳酸盐
C.向醋酸溶液中加入少量氢氧化钠固体,由于发生中和反应,溶液的导电能力降低
D.NaCl溶液能导电所以NaCl溶液是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.滴入酚酞显红色的溶液:Na+、Mg2+、NO 、HSO
、HSO
B.0.1 mol·L-1 Fe(NO3)2溶液:H+、Al3+、SO 、Cl-
、Cl-
C.0.1 mol·L-1氨水溶液:K+、Na+、NO 、AlO
、AlO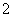
D.由水电离出的c(H+)=10-11 mol·L-1的溶液:Ca2+、NH 、Cl-、HCO
、Cl-、HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
100 g炭粉燃烧所得气体中,CO占2/3、CO2占1/3,且C(s)+1/2O2(g)===CO(g) ΔH=-110.35 kJ/mol,CO(g)+1/2O2(g)===CO2(g) ΔH=-282.57 kJ/mol,与这些炭粉完全燃烧相比损失的热量是( )
A.784.92 kJ B.2 489.44 kJ
C.1 569.83 kJ D.3 274.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:

某小组为研究电化学原理,设计如图装置。下列叙述错误的是( )
A.a和b不连接时,铁片质量会增加
B.a和b用导线连接时,正极发生的电极反应为:Cu2++2e-===Cu
C.无论a和b是否连接,铁片均被腐蚀
D.a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH--4e-===2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
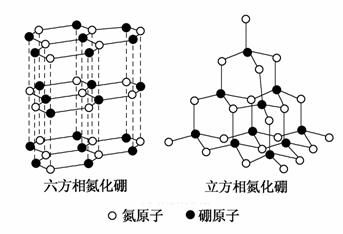
(1)基态硼原子的电子排布式为________。
(2)关于这两种晶体的说法,正确的是________(填选项字母)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B—N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________,其结构与石墨相似却不导电,原因是_________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为__________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是______________________________________________________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有________mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如下:

回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为________________、________________。
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是________,滤渣是________;过滤操作②的滤液是________和________,滤渣是________。
(3)工艺过程中③和④的目的是_________________________________。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是__________________。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。称量草酸成品0.250 g溶于水,用0.050 0 mol·L-1的酸性KMnO4溶液滴定,至浅粉红色不消褪,消耗KMnO4溶液15.00 mL,反应的离子方程式为______________________;列式计算该成品的纯度____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
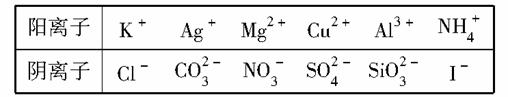
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是________________。
(3)甲同学最终确定原溶液中所含阳离子有________,阴离子有______;并据此推测原溶液应该呈________性,原因是________________________
(请用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为________________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
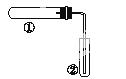
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加 的混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com