
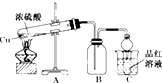
 某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验.
某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验.分析 (1)加热条件下,浓硫酸和Cu发生氧化还原反应生成硫酸铜、二氧化硫和水;
(2)加热条件下,浓硫酸和Cu反应生成二氧化硫,但稀硫酸和铜不反应;
(3)二氧化硫具有漂白性,能使品红溶液褪色;
(4)稀硫酸不和Cu反应;
(5)二氧化硫属于酸性氧化物,能和碱反应生成盐和水;
(6)稀硫酸具有酸性,能和较活泼金属发生置换反应,能和弱酸盐反应生成弱酸.
解答 解:(1)加热条件下,浓硫酸和Cu发生氧化还原反应生成硫酸铜、二氧化硫和水,反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑,故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;
(2)加热条件下,浓硫酸和Cu反应生成二氧化硫,但稀硫酸和铜不反应,且铜和浓硫酸的反应中只有一半的浓硫酸作氧化剂,所以二氧化硫的物质的量是参加反应的浓硫酸物质的量的一半,若用含0.2mlH2SO4的浓硫酸与过量铜片共热,参加反应的浓硫酸的物质的量小于0.2mol,则生成二氧化硫的物质的量小于0.1mol,
故答案为:不能;
(3)二氧化硫能和品红溶液反应生成无色物质而具有漂白性,能使品红溶液褪色,所以C中看到的现象是溶液褪色,故答案为:品红溶液褪色;
(4)加热条件下浓硫酸和Cu反应,而稀硫酸不和Cu反应,所以有一定量的余酸却未能使Cu完全溶解,故答案为:稀硫酸不与铜反应;
(5)二氧化硫属于酸性氧化物,能和碱反应生成盐和水,所以可以在C试管口塞上一团沾有NaOH溶液的棉花,故答案为:NaOH;
(6)稀硫酸具有酸性,能和较活泼金属发生置换反应,能和弱酸盐反应生成弱酸,
A.铁和稀硫酸反应生成氢气,所以该反应能鉴定是否含有稀硫酸,故正确;
B.碳酸钠和稀硫酸反应生成二氧化碳气体,所以该反应能鉴定是否含有稀硫酸,故正确;
C.含有硫酸根离子的溶液都能和氯化钡溶液反应生成白色沉淀,所以该反应不能鉴定是否含有稀硫酸,故错误;
故选AB.
点评 本题以浓硫酸和Cu的反应为载体考查性质实验方案设计,明确实验原理是解本题关键,知道二氧化硫的检验方法,知道实验装置中每个装置的作用,题目难度不大.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
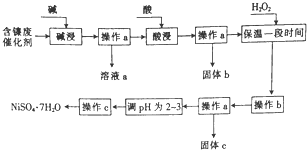 某化学小组通过查阅资料,设计了如图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O,已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
某化学小组通过查阅资料,设计了如图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O,已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| FE(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 颜色 | 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 比热[KJ/kg•℃] |
| Fe | 银白色 | 7.86 | 1 535 | 2 750 | 0.44 |
| Cu | 红色 | 8.92 | 1 083 | 2 567 | 0.38 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学平衡常数表达式是K=$\frac{{c}^{2}(C)•{c}^{2}(D)}{c(A)•c(B)}$ | |
| B. | 若向平衡体系中加入少量生成物C,则正、逆反应速率均增大 | |
| C. | 增大该体系的压强,A的转化率增大 | |
| D. | 该条件下B的平衡转化率是40% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
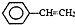 ),聚苯乙烯的化学式为
),聚苯乙烯的化学式为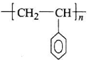
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚二氧化碳塑料是通过加聚反应制得的 | |
| B. | 聚二氧化碳塑料与干冰互为同素异形体 | |
| C. | 聚二氧化碳塑料与干冰都属于纯净物 | |
| D. | 聚二氧化碳塑料的使用会产生白色污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com