
【题目】下列物质既能发生消去反应生成相应的烯烃,又能氧化成相应的醛的是( )
A.CH3OH
B.CH2OHCH2CH3
C.(CH3)2COHCH3
D.(CH3)3COH
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A. 加入KSCN溶液一定不变红色 B. 溶液中一定含Fe2+
C. 溶液中一定不含Cu2+ D. 剩余固体中一定含Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,11.2L的戊烷所含的分子数为0.5NA
B.28g乙烯所含共用电子对数目为4NA
C.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
D.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往100mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M.通入的CO2的体积(标准状况)与M的质量的关系如图所示.试回答下列问题:
(1)A点时,白色固体M的化学式为 , 通入的CO2的体积为mL(标准状况下,下同).
(2)C点时,白色固体M的化学式为 , 通入的CO2的体积为mL.
(3)B点时M的组成成分为(用化学式表示),通入的CO2的体积为mL.
(4)该NaOH溶液的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是 ( )
A.在标准状况下,22.4 L C2H6中含共价键的数目为6 NA
B.5 g KHCO3与CaCO3混合固体中阴离子数目为0.05 NA
C.常温下,1 L 0.1 mol·L–1 CH3COONa溶液中CH3COO-离子数目为0.1 NA
D.在Na2O2与H2O的反应中,当转移0.2 NA个电子时生成的O2体积为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验.
测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度.
实验原理2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置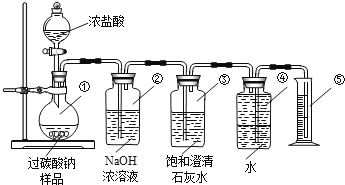
交流与讨论
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品的纯度.
(1)装置②的作用是:;
(2)装置③的作用是:;
(3)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于g;
(4)Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是();(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
(5)Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g.则该样品的纯度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,有以下物质相互转化,其中B溶液为浅绿色,I溶液为棕黄色,J为AgCl,请回答:

(1)C是(填化学式)_____,F的化学式_____.
(2)写出B的化学式______,检验B中阳离子的操作方法是__________________.(只填一种方法,用文字表述)
(3)写出由G转变成H的化学方程式_______________________.
(4)写出检验I溶液中阳离子的离子方程式________________;向I溶液中加入单质Cu的有关离子反应方程式是______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 氯气跟水反应:Cl2+H2O == 2H++Cl-+ClO-
B. 二氧化锰跟浓盐酸共热制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C. 硅与氢氧化钠溶液反应:2Si+2 OH-+2H2O =2SiO32-+3H2↑
D. 向漂白粉溶液中通入过量CO2:Ca2++2ClO-+CO2+H2O == CaCO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某待测溶液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ca2+、Ba2+、NH4+等离子。进行了下述实验(所加酸、碱、氨水、溴水都是过量的)。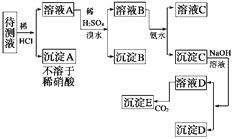
根据实验回答下列问题:
(1)判定待测液中有无Ba2+、Ca2+ , 并写出理由。
(2)写出沉淀D的化学式:。
(3)写出从溶液D生成沉淀E的反应的离子方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com