
�ס��ҡ��������ձ��зֱ�װ��ϡ���ᡢ�Ȼ�ͭ��Һ������ʳ��ˮ�����õ������ӵ�пƬ��ͭƬ����ף��ѷֱ���ֱ����Դ��������������C1��C2�����ң��ѷֱ���ֱ����Դ��������������C3����Ƭ�������������������ȷ���� �� ��
A���ס������ǻ�ѧ��ת��Ϊ���ܣ������ǵ���ת��Ϊ��ѧ��
B��C1��C2�ֱ���������������пƬ����Ƭ�϶�����������Ӧ
C��C1��C3�ų���������ͬ��ͭƬ����Ƭ�ų�������Ҳ��ͬ
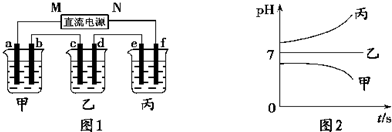
D���ס�������Һ��PHֵ�����ߣ�������Һ��PHֵ��С
C
���⿼��ԭ��غ͵��ص�ԭ�����������֪������ԭ��أ��Һͱ��ǵ��أ�Aѡ����͵�Դ���������ĵ缫�������������Ϸ���������Ӧ���͵�Դ���������ĵ缫�������������Ϸ�����ԭ��Ӧ������C1��C2�ֱ�����������������Ƭ��Ϊ������������ԭ��Ӧ��пƬ��Ϊԭ��صĸ���������������Ӧ��Bѡ������ܷ�Ӧ��Zn��2H��=Zn2����H2����pH�������ǵ���Ȼ�ͭ��Һ��pH�����ǵ�ⱥ��ʳ��ˮ������NaOH��pH����Dѡ�����


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
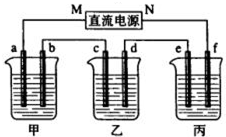 ��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��109g5.51%��NaOH��Һ��������CuSO4��Һ��200g10.00%��K2SO4��Һ���缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47%������c�缫�������ӣ��ݴ˻ش����⣺
��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��109g5.51%��NaOH��Һ��������CuSO4��Һ��200g10.00%��K2SO4��Һ���缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47%������c�缫�������ӣ��ݴ˻ش����⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||

| ���� |
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�긣��ʡ�����и�һ��ѧ��������⻯ѧ���� ���ͣ�ʵ����
Ϊ�ⶨþ���Ͻ𣨲�������Ԫ�أ������������������ס��ҡ�������ѧϰС��������������ֲ�ͬ��ʵ�鷽������̽������ش��������⣺ ��һ�����飺ʵ�鷽����þ���Ͻ�
��һ�����飺ʵ�鷽����þ���Ͻ� �ⶨʣ���������
�ⶨʣ���������
ʵ�鲽�裺
�ٳ������� ����ƽ����һ������þ���Ͻ��ĩ
����ƽ����һ������þ���Ͻ��ĩ
���ܽ⣺������ҩƷ�����ձ��У����������NaOH��Һ�����Ͻ��裬��ַ�Ӧ��������Ӧ�����ӷ���ʽΪ
�۹��ˣ�
��ϴ�ӣ���δ�Թ������ù������ϴ�ӣ������������������ ���ƫ�ߡ�����ƫ�͡����䡱��
�ݸ������ʣ����� ���������飺ʵ�鷽����þ���Ͻ�
���������飺ʵ�鷽����þ���Ͻ� �ⶨ������������
�ⶨ������������
ʵ��װ��������ͼ
��1��ijͬѧ�����ʵ��װ�ò������ƣ�Ӧ��A��B֮������һ��װ�м�ʯ�ҵĸ���װ�á��������� �����Ҫ������Ҫ����
��2��Ϊʹ�ⶨ��������ܾ�ȷ��ʵ����Ӧע��������ǣ�Ҫ��д�����㣩 ��
���������飺ʵ�鷽����12 gþ���Ͻ�
����l�������ˡ�ϴ�ӡ�����ͳ����� �����յõ���������1��45g����úϽ���������������Ϊ ��
�����յõ���������1��45g����úϽ���������������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�긣��ʡ�����и�һ��ѧ��������⻯ѧ���� ���ͣ�ʵ����
Ϊ�ⶨþ���Ͻ𣨲�������Ԫ�أ������������������ס��ҡ�������ѧϰС��������������ֲ�ͬ��ʵ�鷽������̽������ش��������⣺
��һ�����飺ʵ�鷽����þ���Ͻ� �ⶨʣ���������
�ⶨʣ���������
ʵ�鲽�裺
�ٳ�����������ƽ����һ������þ���Ͻ��ĩ
���ܽ⣺������ҩƷ�����ձ��У����������NaOH��Һ�����Ͻ��裬��ַ�Ӧ��������Ӧ�����ӷ���ʽΪ
�۹��ˣ�
��ϴ�ӣ���δ�Թ������ù������ϴ�ӣ������������������ ���ƫ�ߡ�����ƫ�͡����䡱��
�ݸ������ʣ�����
 ���������飺ʵ�鷽����þ���Ͻ�
���������飺ʵ�鷽����þ���Ͻ� �ⶨ������������
�ⶨ������������
ʵ��װ��������ͼ
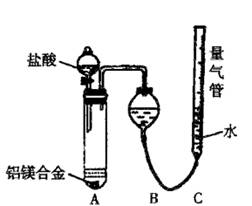
��1��ijͬѧ�����ʵ��װ�ò������ƣ�Ӧ��A��B֮������һ��װ�м�ʯ�ҵĸ���װ�á��������� �����Ҫ������Ҫ����
��2��Ϊʹ�ⶨ��������ܾ�ȷ��ʵ����Ӧע��������ǣ�Ҫ��д�����㣩 ��
���������飺ʵ�鷽����12 gþ���Ͻ�
����l�������ˡ�ϴ�ӡ�����ͳ����������յõ���������1��45g����úϽ���������������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com