
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
分析 A.煤的干馏和煤的液化都是化学变化;
B.海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多;
C.蚕丝是天然纤维;
D.活性炭脱色是利用其吸附性.
解答 解:A.煤的干馏是指将煤隔绝空气加强热使之分解的过程,煤液化生成甲醇,属于化学变化,故A错误;
B.海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),蒸馏是分离和提纯液态混合物常用的方法之一蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备;离子交换法是用阳离子交换树脂(HR)和水中的金属离子Mn+进行交换的一种方法,通常通过阳离子交换树脂可以除去钙离子和镁离子得到软水,不是历史最久、技术和工艺较完善的主要方法;电渗析法是一种利用离子交换膜进行离子交换的方法,是近年发展起来的一种较好的海水淡化技术,原理为通电后,阴离子移向阳极,阳离子移向阴极,分离盐和水,故B正确;
C.蚕丝是天然纤维,成分为蛋白质,合成纤维的成分是化学纤维,如聚乙烯,故C错误;
D.活性炭脱色是利用其吸附性,次氯酸盐漂白是利用次氯酸的强氧化性,故D错误.
故选B.
点评 本题考查化学与生活、环境的关系,为高考常见考题,为理综中化学选择题首先出现的习题,涉及知识面较广,侧重分析与应用、化学与生活、环境等综合知识的考查,题目难度不大.


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ③④⑤ | C. | ②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1丙醇 | B. | 乙醇 | C. | 1丁醇 | D. | 1戊醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
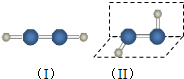 过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:
过氧化氢是应用广泛的“绿色”氧化剂,酸性条件下稳定,中性或弱碱性条件下易分解.填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键的类型由元素的类别决定 | |
| B. | 不同种元素组成的多原子分子里的化学键一定是极性键 | |
| C. | 阴、阳离子相互反应形成的化学键称为离子键 | |
| D. | 熔融态下能导电的化合物中一定含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 操作及现象 |
| ⅰ | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ⅱ | 向ⅰ中所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液至过量,产生无色气体(经检验为O2),溶液变为深红色,且红色很快褪去 |
| 实验序号 | 操作、现象 |
| ⅲ | 将ⅱ中剩余溶液均分为两份,一份滴加NaOH溶液,产生红褐色沉淀; 另一份滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀不溶解 |
| ⅳ | 取2mL 0.1mol/L FeCl3溶液,滴入KSCN溶液,溶液变为红色,通入一段时间O2, 无明显变化.再加入H2O2溶液,红色很快褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
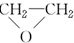 (环氧乙烷).
(环氧乙烷).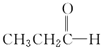 $\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH
$\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH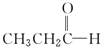 $→_{HCl}^{Zn(Hg)}$CH3CH2CH3
$→_{HCl}^{Zn(Hg)}$CH3CH2CH3查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤和结论(不要求写具体操作过程): |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com