
下列有机反应的叙述中,错误的是( )
A.甲苯与氯气在光照下反应主要生成2,4,6?三氯甲苯
B.苯乙烯在一定条件下催化加氢可生成乙基环己烷
C.乙烯与溴水反应生成1,2?二溴乙烷
D.苯与浓硝酸、浓硫酸共热并保持55~60 ℃反应生成硝基苯
科目:高中化学 来源:2015-2016学年河北省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列反应可以设计成原电池的是( )
①CaO+H2O===Ca(OH)2 ②Fe+H2SO4===FeSO4+H2↑
③2H2O===2H2↑+O2↑ ④NaCl+AgNO3===AgCl↓+NaNO3
⑤Cu+2AgNO3===2Ag+Cu(NO3)2 ⑥Fe+2FeCl3===3FeCl2
A.①②④⑤⑥ B.②③⑤⑥ C.②⑤⑥ D.全部
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高二下学期期中考试化学试卷(解析版) 题型:选择题
有关晶体的下列说法中正确的是( )
A.分子晶体中共价键越强,熔点越高 B.原子晶体中分子间作用力越强,熔点越高
C.氯化钠晶体熔化时离子键发生断裂 D.金属晶体熔化时金属键未发生断裂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为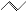 。有机物X的键线式为
。有机物X的键线式为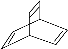 ,下列说法正确的是( )
,下列说法正确的是( )
A.X的化学式为C8H10
B.有机物Y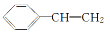 与X互为同系物
与X互为同系物
C.X因发生加成反应而使酸性高锰酸钾溶液褪色
D.X与足量的H2在一定条件下反应可生成环状烃Z,Z的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下学期期中考试化学试卷(解析版) 题型:选择题
除去下列有机物中的杂质,所选试剂正确的是(括号中的是杂质)( )
A.乙烯(乙炔):酸性高锰酸钾溶液
B.溴苯(苯):液溴、铁粉
C.乙烷(乙烯):氢气、镍
D.苯(甲苯):酸性高锰酸钾溶液、氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下学期期中考试化学试卷(解析版) 题型:填空题
乙二醇(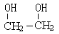 )是一种重要的化工原料,
)是一种重要的化工原料,
Ⅰ.在一定条件下以CO和H2为原料可以合成乙二醇,反应方程式如下:
2CO(g)+3H2(g) 
 (g) ΔH= a kJ/mol
(g) ΔH= a kJ/mol
(1)该反应能够自发进行,可以推出a 0;(填“>”“<”或“=”)。
(2)在一定温度下,向体积为1L的恒容密闭容器中充入2 mol CO (g)和3mol H2(g),压强为P1,达到平衡时压强变为P2,且P1:P2=15:7,则该温度下的化学平衡常数K=______
(3)只改变反应的一个条件,能使平衡体系中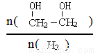 增大的措施有 (写两条)
增大的措施有 (写两条)
Ⅱ.乙二醇经连续催化氧化后可得到乙二酸(HOOC-COOH),乙二酸俗称草酸,分子式可以用H2C2O4表示,H2C2O4是一种二元弱酸,常温下其电离平衡常数K1=5.0×10-2,K2=5.0×10-5
(1)H2C2O4的电离方程式为 。
(2)Na2C2O4溶液显 (填“酸性”、“中性”或“碱性”),溶液中各离子浓度从大到小的顺序为 。
(3)已知常温下NH3·H2O的电离平衡常数K=1.75×10-5,常温下,
反应NH3·H2O + HC2O4-  NH4+ +C2O42-+H2O的平衡常数K= 。
NH4+ +C2O42-+H2O的平衡常数K= 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下学期期中考试化学试卷(解析版) 题型:选择题
甲酸甲酯和甲酸的混合物中,氧元素的质量分数为65%,则碳元素的质量分数为
A.15% B.20% C.25% D.30%
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练五化学试卷(解析版) 题型:实验题
醋酸亚铬水合物{[Cr(CH3COO)2]2•2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂.实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如右图所示,且仪器2中预先加入锌粒.已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:
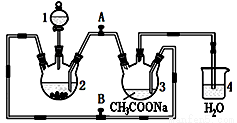
Zn(s)+2HCl(aq)═ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)═2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)═[Cr(CH3COO)2]2•2H2O(s)
请回答下列问题:
(1)仪器1的名称是_____________。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是_____________(选下面的A、B或C);目的是_____________。
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门_____________(填“A”或“B”,下同),打开阀门_____________。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是_____________。
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[Cr(CH3COO)2]2•2H2O 9.4g,则该实验所得产品的产率为_____________(不考虑溶解的醋酸亚铬水合物)。
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的_____________,再加入碱液,调节pH至少为_____________才能使铬的离子沉淀完全(铬的离子浓度应小于10-5mol/L).已知Cr(OH)3的溶度积为6.3×10-31,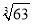 ≈4,lg2≈0.3
≈4,lg2≈0.3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
已知aAn+、bB(n+1)+、cCn﹣、dD(n+1)﹣均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
A.原子半径:A>B>C>D B.原子序数:b>a>c>d
C.离子半径:D>C>B>A D.金属性:B>A,非金属性:D>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com