
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH 1=+489.0 kJ·mol-1
C(s) + CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g) HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g) CH3OH(g)+CO(g) △H>0
CH3OH(g)+CO(g) △H>0
①第一步反应的机理可以用下图表示:
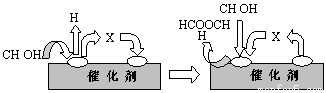
图中中间产物X的结构简式为 。
②在工业生产中,为提高CO的产率,可采取的合理措施有 。(写两条措施)
(3)第21届联合国气候变化大会(COP21)于2015年11月30日至12月11日在巴黎召开。会议旨在讨论控制温室气体CO2的排放,减缓全球变暖,力争将全球气温上升控制在2度内。
①Li4SiO4可用于富集得到高浓度CO2。原理是:在500℃,低浓度CO2与Li4SiO4接触后生成两种锂盐;平衡后加热至700℃,反应逆向进行,放出高浓度CO2,Li4SiO4再生。请写出700℃时反应的化学方程式为: 。
②利用太阳能和缺铁氧化物[如Fe0.9O]可将富集到的廉价CO2热解为碳和氧气,实现CO2再资源化,转化过程如下图所示,若用1mol缺铁氧化物[Fe0.9O]与足量CO2完全反应可生成 molC(碳)。

③固体氧化物电解池(SOEC)用于高温电解CO2/H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如下图。
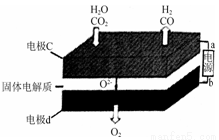
写出电极c上发生的电极反应式: , 。
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见下图。

如何解释图中250-400℃时温度升高与乙酸的生成速率变化的关系? 。
科目:高中化学 来源:2015-2016学年浙江省金兰教育合作组织高一上学期期中联考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25oC,1.01×105Pa,64gSO2中含有的原子数为3NA
C.在常温常压下,11.2LCl2含有的分子数为0.5NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源:2016届广东省七校联合体高三上学期第二次联考理综化学试卷(解析版) 题型:推断题
醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展,其结构简式为:
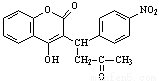
醋硝香豆素可以通过以下方法合成(部分反应条件省略)。
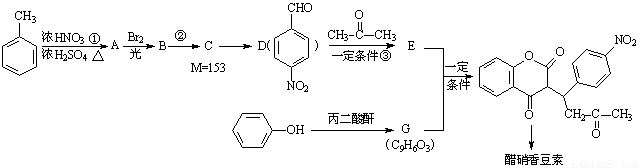
已知: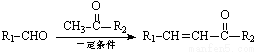 + H2O
+ H2O
回答以下问题:
(1)反应①的反应类型是 。
(2)从A到B引入的官能团名称是 。
(3)反应②的化学方程式为 。
(4)反应③的化学方程式为 。
(5)关于E物质,下列说法正确的是 (填字母序号)。
a.在核磁共振氢谱中有四组吸收峰
b.可以用酸性高锰酸钾溶液鉴别D和E
c.可以发生加成反应、聚合反应、氧化反应和还原反应
d.存在顺反异构
(6)写出G的结构简式 。
(7)分子结构中只含有一个环,且同时符合下列条件的G的同分异构体共有 种。
①可与氯化铁溶液发生显色反应;
②可与碳酸氢钠溶液反应生成二氧化碳气体。
其中,苯环上的一氯代物只有两种的同分异构体的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
含有下列各组离子的溶液中,通入过量SO2气体后仍能大量共存的是
A.H+、Ca2+、Fe3+、NO3- B.Ba2+、Cl-、Al3+、H+
C.K+、NH4+、I-、HS- D.Na+、CO32-、K+、NO3-
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上第二次阶段测化学试卷(解析版) 题型:推断题
化合物F是一种常见的化工原料,可以通过以下方法合成:

(1)写出化合物C中含氧官能团的名称: 和 。
(2)化合物B的结构简式为 ;由D→E的反应类型是 。
(3)写出C→D反应的化学方程式: 。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式: 。
Ⅰ.能发生银镜反应 ; Ⅱ.水解产物之一遇FeCl3溶液显色;
Ⅲ.分子中含有4种不同化学环境的氢。
(5)已知 。请写出以
。请写出以 为原料,制备化合物
为原料,制备化合物 的合成路线流程图(无机试剂可任选)。
的合成路线流程图(无机试剂可任选)。
合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:填空题
(1)已知H-H 键能为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据化学方程式: N2(g)+3 H2(g)=2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是
(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是__________________。
A.C(s) + H2O(g) = CO(g) + H2(g) △H > 0
B.2H2(g)+O2(g)=2H2O(1) △H < 0
C.NaOH(aq) + HC1(aq) = NaC1(aq) + H2O(1) △H < 0
(3)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式__________。
(4)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
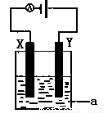
① 若a为CuSO4溶液,则电解时的化学反应方程式为 。
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672 mL(标准状况下)时,溶液的pH=_______________(假设电解后溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列制作铅笔的材料与相应工业不对应的是
A.橡皮擦——橡胶工业 B.铝合金片——冶金工业
C.铝笔芯—电镀工业 D.铅笔漆—涂料工业
查看答案和解析>>
科目:高中化学 来源:2016届四川省自贡市高三上第一次诊断考试理综化学试卷(解析版) 题型:选择题
某有机化合物的结构简式为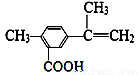 ,有关该化合物的叙述不正确的是
,有关该化合物的叙述不正确的是
A.该有机物的分子式为C11H12O2
B.lmol该物质最多能与4molH2发生加成反应
C.该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀
D.该有机物一定条件下,可以发生取代、氧化、酯化反应
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖江名校高三上学期12月联考化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.月饼等食品常在包装中放人生石灰做脱氧剂
B.埃博拉病毒能够通过气溶胶传播,病毒颗粒直径大约为80nm
C.纤维素可水解成葡萄糖,故可为人体提供营养
D.用Na2FeO4处理污水,可杀菌消毒,但不能沉降水中的悬浮物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com