
| A�� | �� | B�� | �١��� | C�� | �١��ڡ��� | D�� | �١��ڡ��ۡ��� |
���� ��Ʒ��������ϵͳ����Χ��ϵͳ���кܴ�����ɲ����쳣���˷ܡ����Ƶ����ã�����һϵ��������֢״����ʧ�ߡ����ꡢ���ʡ���ԡ��������½��������Խ��͡��Ը��Ƨ����־��������Χ���ȣ�����Ѫ��ϵͳ������ϵͳ������ϵͳ����ֳϵͳ�ȶ���������ص�Σ������Ʒ���к�ǿ�ij���ԣ�һ��մȾ�����ѽ��������Σ���������Ľ�����Σ����ᣮһ���١��ٶ����������γ��˶Զ�Ʒ��������֮��������Ŀ�л�ϵݼ�����ˣ�Ϊ�˴ﵽ��ԭ��ͬ���Ĵ̼�ǿ�ȣ������߱���Ӵ�����������Ʒ�������Ȼ�������ʳ�����������������룮
��� �⣺��ʳ��Ʒ�ɲ����쳣���˷ܡ����Ƶ����ã�����һϵ��������֢״����ʧ�ߡ����ꡢ���ʡ���ԡ��������½��������Խ��͡��Ը��Ƨ����־��������Χ���ȣ���Ʒ���к�ǿ�ij���ԣ�����þ���˼ά�ϰ�������ע�䶾Ʒ�������ߴ�����Ⱦ�Ժϲ�֢��
��ѡD��
���� ���⿼��ҩ�����Ҫ�ɷֺ���Ч���Ƚϻ��������ضԻ���֪ʶ�Ĺ��̣�ע��Ի���֪ʶ���������գ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 2.3g������ȫ�����������ʱʧȥ�ĵ�����ĿΪ0.2NA | |
| B�� | 2g����������ԭ����ĿΪNA | |
| C�� | 17gNH3�����ĵ�����Ϊ10NA | |
| D�� | NA�������Ӻ�NA������ӵ������ȵ���16��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO3-��Ag+��H+��Cl- | B�� | CO32-��Na+��Ca2+��NO3- | ||
| C�� | Mg2+��Cl-��OH-��CH3COO- | D�� | Mg2+��SO42-��K+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ƶ�Ŀ�������ж�ɱ���õ����͡��ɽ���ɱ��� | |
| B�� | ������չũ���������������Ľո�ת��Ϊ����Ч����Դ | |
| C�� | ���ƿ�����ˮ�����л��ܼ��Ļ���Ϳ�� | |
| D�� | �Ծ۱���ϩȫ�����ľ�ģ�������װ�С���ͺе��Լ���ľ��ʹ�ã�����ɭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪H2�ı�ȼ���ȡ�H=-285.8 kJ•mol-1�������Ȼ�ѧ����ʽ�ɱ�ʾΪ��H2��g��+1/2O2��g���TH2O��g����H=-285.8 kJ•mol-1 | |
| B�� | ��NH4A1��SO4��2��Һ�е���Ba��OH��2��Һǡ��ʹSO42-������ȫ��2Ba2++4OH-+Al3++2SO42-�T2BaSO4��+AlO2-+2H2O | |
| C�� | ��֪�к���Ϊ57.3 kJ•mol-1��ϡ��������������ϡ��Һ��Ӧ���Ȼ�ѧ����ʽ��H2SO4 ��aq��+2NaOH ��aq���TNa2SO4 ��aq��+2H2O �� l ����H=-114.6 kJ•mol-1 | |
| D�� | ��ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3�T2FeO42-+3Cl-+H2O+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
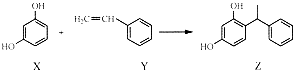
| A�� | X��Z������FeCl3 �γ���ɫ����Һ | |
| B�� | 1molZ���������3mol��ˮ | |
| C�� | Y���ܷ���ȡ����Ӧ��Ҳ�ܷ����ӳɷ�Ӧ | |
| D�� | Y�����Ӿ۷�Ӧ���壬X�������۷�Ӧ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com