
”¾ĢāÄæ”æĻņÅضČĻąµČ”¢Ģå»ż¾łĪŖ50mlµÄA”¢BĮ½·ŻĒāŃõ»ÆÄĘČÜŅŗÖŠ·Ö±šĶØČėŅ»¶ØĮæµÄ¶žŃõ»ÆĢ¼ŗó£¬ŌŁĻ”ŹĶÖĮ100ml”£
£Ø1£©ĻņĒāŃõ»ÆÄĘČÜŅŗÖŠĶØČėŅ»¶ØĮæµÄ¶žŃõ»ÆĢ¼ŗó£¬ČÜŅŗÖŠČÜÖŹµÄæÉÄÜ×é³ÉÓŠ£ŗ¢Ł______£»¢Ś_______£»
¢Ū_______£»¢Ü_______”£
£Ø2£©ĻņĻ”ŹĶŗóµÄČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/LµÄŃĪĖįČÜŅŗ£¬²śÉś¶žŃõ»ÆĢ¼µÄĢå»ż(±ź×¼×“æö)ÓėĖł¼ÓŃĪĖįČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾”£
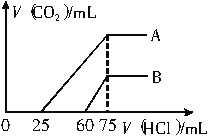
¢ŁAĒśĻß±ķĆ÷£¬ĻņŌČÜŅŗÖŠĶØČė¶žŃõ»ÆĢ¼ŗó£¬ĖłµĆČÜÖŹÓėHCl·“Ó¦²śÉś¶žŃõ»ÆĢ¼µÄ×ī“óĢå»żŹĒ_______mL(±ź×¼×“æö)”£
¢ŚBĒśĻß±ķĆ÷£¬ĻņŌČÜŅŗÖŠĶØČė¶žŃõ»ÆĢ¼ŗó£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄ»ÆѧŹ½ĪŖ___________”£
¢ŪŌĒāŃõ»ÆÄĘČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ__________”£
”¾“š°ø”æ(10·Ö)£Ø1£©¢ŁNaOH”¢Na2CO3£»¢ŚNa2CO3£»¢ŪNa2CO3”¢NaHCO3£»¢ÜNaHCO3(4·Ö)
£Ø2£©¢Ł112(2·Ö)¢ŚNaOH”¢Na2CO3(2·Ö)¢Ū0.15mol/L(2·Ö)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©ÓÉCO2+2NaOHØTNa2CO3+H2O”¢CO2+NaOHØTNaHCO3£¬¶žŃõ»ÆĢ¼ÉŁĮæŹ±¹ĢĢåĪŖ¢ŁNa2CO3ŗĶNaOH£»ŅŌ1£ŗ2Ē”ŗĆ·“Ó¦Ź±ĪŖ¢ŚNa2CO3£»ĪļÖŹµÄĮæ±Č½éÓŚ1£ŗ1”«1£ŗ2Ö®¼äĪŖ¢ŪNa2CO3ŗĶNaHCO3£»¶žŃõ»ÆĢ¼¹żĮæŹ±ĪŖ¢ÜNaHCO3£»
£Ø2£©ÓÉĶ¼æÉÖŖ£¬¶ŌÓ¦BČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį60mLŹ±Ć»ÓŠĘųĢåÉś³É£¬æÉÄÜ·¢ÉśOH-+H+=H2OŗĶCO32-+H+=HCO3-£¬¼ŁÉčŌČÜŅŗÖŠÖ»ÓŠĢ¼ĖįÄĘ£¬Éś³ÉĢ¼ĖįĒāÄĘŠčŅŖŃĪĖįµÄĢå»żŗĶĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»żĻąµČ£¬Źµ¼ŹÉĻŠčŅŖŃĪĖįµÄĢå»ż60mLŌ¶Ō¶“óÓŚĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»ż(75-60)mL=15mL£¬ĖµĆ÷ŌČÜŅŗÖŠµÄČÜÖŹŹĒNaOHŗĶNa2CO3£»¶ŌÓŚAČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį25mLŹ±Ć»ÓŠĘųĢåÉś³É£¬æÉÄÜ·¢ÉśOH-+H+=H2OŗĶCO32-+H+=HCO3-£¬¼ŁÉčŌČÜŅŗÖŠÖ»ÓŠĢ¼ĖįÄĘ£¬Éś³ÉĢ¼ĖįĒāÄĘŠčŅŖŃĪĖįµÄĢå»żŗĶĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»żĻąµČ£¬Źµ¼ŹÉĻŠčŅŖŃĪĖįµÄĢå»ż25mLŠ”ÓŚĢ¼ĖįĒāÄĘÉś³ÉĀČ»ÆÄĘŠčŅŖŃĪĖįµÄĢå»ż(75-25)mL=50mL£¬ĖµĆ÷ŌČÜŅŗÖŠµÄČÜÖŹŹĒNa2CO3ŗĶNaHCO3£¬
¢Ł¶ŌÓŚAČÜŅŗĄ“Ėµ£¬µĪ¼ÓŃĪĖį25mLŹ±ÓŠĘųĢåÉś³É£¬ÖšµĪ¼ÓČė0.1molL-1 µÄŃĪĖį£¬µ±Éś³ÉCO2ĘųĢåŹ±£¬·¢Éś·“Ó¦HCO3-+H+=H2O+CO2”ü£¬
ŌņHCO3-+H+=H2O+CO2”ü
1 1
n(CO2)=0.05L”Į0.1mol/L=0.005mol£¬±źæöĻĀĢå»żĪŖ0.005mol”Į22.4L/mol=0.112L=112mL£»
¢ŚÓÉÉĻŹö·ÖĪöæÉÖŖ£¬BÖŠČÜÖŹŹĒNa2CO3ŗĶNaOH£¬ÓÉĻūŗÄŃĪĖįµÄ¹ŲĻµæÉÖŖ£¬ĪļÖŹµÄĮæ±ČĪŖ3£ŗ1£»
¢Ū¼ÓČė×ćĮæµÄŃĪĖįŗóµÄČÜŅŗÖŠ¾łÖ»“ęŌŚNaCl£¬n(HCl)=n(NaOH)=0.075L”Į0.1mol/L=0.0075mol£¬c(NaOH)=n/V=0.0075mol”Ā0.05L=0.15mol/L”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A. ŅŅĶé¹āÕÕĻĀÄÜÓėÅØŃĪĖį·¢ÉśČ”“ś·“Ó¦
B. ŅŅĻ©æÉŅŌÓĆ×÷Éś²śŹ³Ę·°ü×°²ÄĮĻµÄŌĮĻ
C. ŅŅ“¼ŹŅĪĀĻĀŌŚĖ®ÖŠµÄČܽā¶Č“óÓŚäåŅŅĶé
D. ŅŅĖįŗĶ¼×Ėį¼×õ„»„ĪŖĶ¬·ÖŅģ¹¹Ģå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾£¬²»ÄÜŹŹÓĆÓŚĻĀĮŠæÉÄę·“Ó¦µÄŹĒ
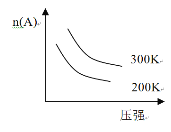
A£®3A£Øg£©+B£Øg£©![]() 2C£Øg£©£»¦¤H<0
2C£Øg£©£»¦¤H<0
B£®A£Øg£©+3B£Øs£©+2C£Øg£©![]() 3D£Øg£©£»¦¤H<0
3D£Øg£©£»¦¤H<0
C£®C£Øs£©+D£Øg£©![]() A£Øg£©+B£Øg£©¦¤H>0
A£Øg£©+B£Øg£©¦¤H>0
D£®2C£Øg£©![]() 2A£Øg£©+B£Øg£©¦¤H>0
2A£Øg£©+B£Øg£©¦¤H>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö±š½«×ćĮæĻĀĮŠĘųĢåĶØČėĻ”Na2SČÜŅŗÖŠ£¬æÉŅŌŹ¹ČÜŅŗ±ä»ė×ĒµÄŹĒ
A£®CO B£®SO2 C£®HCl D£®CO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ( )
A£®ŗ¬ÓŠNAøöŗ¤Ō×ÓµÄŗ¤ĘųµÄĪļÖŹµÄĮæĪŖ2Ħ¶ū
B£®2Ħ¶ūĖ®µÄĦ¶ūÖŹĮæŹĒ1Ħ¶ūĖ®µÄĦ¶ūÖŹĮæµÄ2±¶
C£®25 ”ę£¬1.01”Į105Pa, 64gµÄSO2ÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ3NA
D£®lĦ¶ūČĪŗĪĪļÖŹĖłŗ¬µÄ·Ö×ÓŹż¾łĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠŗ¬ÓŠĄė×Ó¼üµÄŹĒ
A. Cl2 B. Na2O2 C. CO 2 D. NH3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚ½šŹōµÄĖµ·ØÖŠ²»ÕżČ·µÄŹĒ(””””)
A. ŗĻ½š±Č“潚Źō¾ßÓŠ½ĻŗƵĊŌÄÜ£¬Ņ»°ćĒéæöĻĀ£¬Ó²¶Č±Č“潚Źōøߣ¬ČŪµć±Č“潚ŹōµÄµĶ
B. ŗĻ½šČŌČ»¾ßÓŠ½šŹōĢŲŠŌ
C. ³£ÓƵē½ā·ØŅ±Į¶ÄĘ”¢Ć¾”¢ĀĮµČ»īĘĆ½šŹō
D. ½«øÖÕ¢ĆÅÓėµēŌ“Õż¼«ĻąĮ¬£¬æÉ·ĄÖ¹ĘäŌŚŗ£Ė®ÖŠ±»øÆŹ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬½«°±Ė®ÓėĀČ»Æļ§ČÜŅŗ»ģŗĻµĆµ½c(NH3”¤H2O)+c(NH4+)=0.1 mol”¤L-1µÄ»ģŗĻČÜŅŗ”£ČÜŅŗÖŠc(NH3”¤H2O)”¢c(NH4+)ÓėpHµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲĄė×ÓÅØ¶Č¹ŲĻµŠšŹöŅ»¶ØÕżČ·µÄŹĒ( ) 
A£®Wµć±ķŹ¾ČÜŅŗÖŠ£ŗc(NH4+)+c(H+)=c(OH-)
B£®pH=10.5ČÜŅŗÖŠ£ŗc(Cl-)+c(OH-)+c(NH3”¤H2O)<0.1 mol”¤L-1
C£®pH=9.5ČÜŅŗÖŠ£ŗc(NH3”¤H2O)>c(NH4+)>c(OH-)>c(H+)
D£®ĻņWµćĖł±ķŹ¾µÄ1 LČÜŅŗÖŠ¼ÓČė0.05 mol NaOH¹ĢĢå(ŗöĀŌČÜŅŗĢå»ż±ä»Æ)£ŗc(Cl-)>c(Na+)>c(OH-)>c(N H4+)>c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČÜŅŗÖŠ¼ÓČė×ćĮæNa2O2ŗóČŌÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ
A. NH![]() ”¢Ba2£«”¢Cl£”¢NO
”¢Ba2£«”¢Cl£”¢NO![]()
B. K£«”¢AlO![]() ”¢Cl£”¢SO
”¢Cl£”¢SO![]()
C. Ca2£«”¢Mg2£«”¢NO![]() ”¢HCO
ӢHCO![]()
D. Na£«”¢Cl£”¢CO![]() ”¢SO
ӢSO![]()
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com